Гидроперекись - тетралин
Cтраница 2
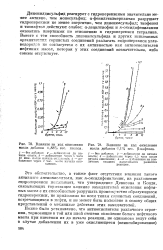
Медведев, Корицкая и Алексеева [32] показали, что при полимеризации хлоропрена под влиянием перекиси бензоила или гидроперекиси тетралина каждая растущая цепь является свободным радикалом. Качественно свободные радикалы были обнаружены по выделению иода из йодистого водорода, а количественно - по присоединению иода. В процессе реакции число свободных радикалов возрастает ( рис. 17) вследствие увеличения вязкости среды, затрудняющей взаимодействие радикалов друг с другом ( обрыв цепи), а также вследствие разветвления реакционных цепей. [16]
В ряде недавно опубликованных работ были сделаны попытки определить влияние различных промоторов - органических гидроперекисей ( например, гидроперекиси тетралина), сложных эфиров надкислот ( например, сложного эфира mpe / n - бутилового спирта и надбензойной кислоты) или циклопарафинов и олефинов на кинетику образования гидроперекиси кумола. [17]
В ряде недавно опубликованных работ были сделаны попытки определить влияние различных промоторов - органических гидроперекисей ( например, гидроперекиси тетралина), сложных эфиров надкислот ( например, сложного эфира mpem - бутилового спирта и надбензойной кислоты) или циклопарафинов и олефинов на кинетику образования гидроперекиси кумола. [18]
До работ Иванова были известны только три выделенных и более ли менее изученных промежуточных вещества перекисно-го характера - гидроперекиси тетралина, циклопентена и цикт логексена. [19]
Так, например, в наибольшей степени задерживают окисление вазелинового масла тио - - нафтол и динонилдисульфид, способность которых разлагать гидроперекись тетралина в 3 - 4 раза ниже таковой фенилэтилмеркаптана и динонил сульфида, не обладающих антиокислительной активностью. [20]
Через жидкий тетралин, содержащий 0 33 % тонко раздробленного карбоната окисиой меди в качестве катализатора и желательно небольшое количество инициатора - гидроперекиси тетралина, пропускают при 90 С в продолжение 3 5 ч сжатый воздух. Смесь, содержащую 41 % гидроперекиси, перемешивают с 15 % - ным NaOH при 80 С и отделяют водный слой. Из органического слоя фракционированной перегонкой при остаточном давления 10 - 25 ми отделяют тетралин, после чего оставшуюся смесь примерно равных количеств а-тетралона и а-тетралола ( общий выход 82 % на вошедший в реакцию тетралин) также перегоняют. Перегнанную смесь гидрируют при 90 - 110 С под давлением в присутствии 5 % катализатора, состоящего из окиси меди и окиси хрома; в продуктах реакции содержится 3 9 % тетралина, который отделяют перегонкой в вакууме. [21]
Это подтверждается наблюдением, согласно которому добавление перекисей кумола или тетралина первоначально уменьшает продолжительность защитного действия, а смесь хлорного железа с гидроперекисью тетралина сильно тормозит аутоокислемие циклогексена. [22]
Более подробные данные об этой реакции содержатся в работе [326], авторами которой исследовано окисление четырех экранированных тризамещенных фенолов с помощью ГПК, ГПТБ, а также гидроперекисей тетралина и дифенилметилметана. Окисление ионола избытком ГПТБ или ГПК приводит к стильбенхинону ( XXX), тогда как из 2-трет. [23]
Эти вещества должны быть достаточно активны, чтобы легко распадаться на свободные радккалы при реакционных условиях - В качестве инициаторов обычно используют различные перекиси как-то: гидроперекись кумола, гидроперекись тетралина, перекись водорода, перекись дитрэтично-го бутила, гидроперекись третичного бутила, перекись бензоила, био-2 - фенил-пропил-перекись - 2, перекись натрия, перекись ацетила, перацетат третичного бум да, персульфат калия, o d - азо-диизобутиронитрил и другие подобные соединения. [24]
 |
Влияние на ход окисления масла добавки 0 88 % вес. ионола.| Влияние на ход окисления. [25] |
Динонилдисульфид реагирует с гидроперекисями значительно менее активно, чем моносульфид; а-фенилэтилмеркаптан разрушает гидроперекиси не менее энергично, чем динонилсульфид; тиофеяол и тионафтол действуют слабее; а-децилтиофен и к-оксидифениламин оказались инертными по отношению к гидроперекиси тетралина. Вместе с тем способность динонилсульфида и других испытанных органических сернистых соединений разлагать гидроперекиси углеводородов не согласуется с их активностью как антиокислителей нефтяных масел, которая у этих соединений незначительна, либо овеем отсутствует. [26]
Существование реакции, подобной ( XIV), было экспериментально показано Налбандяном и Фок [38] при фотохимическом окислении пропана, тогда как реакция ( XV) была предложена Робертсоном и Уотерсом для объяснения образования кислорода при распаде гидроперекиси тетралина. На основе количественных данных Березин, Денисов и Эмануэль [39] пришли к выводу, что в условиях их опытов вместо гидроперекиси основным первичным продуктом является циклогексанон. Относительно циклогексанола они полагали, что в первые 5 - 40 мин он образуется из гидроперекиси, а позднее помимо нее. Независимо от того, как эти реакции могут осуществиться, вопрос о существовании основной цепи окисления, не включающей стадию гидроперекисей, может быть решен только с помощью КИМ. [27]
Перекись трет-бутила, гидроперекись трет-бутила, содержащая не менее 20 % самой перекиси и 20 % флегматизатора; эфир трет-бутиловой надуксусной кислоты, содержащий менее 30 % флег-матизатора; эфир трет-бутиловой надмаленновой кислоты, содержащей не менее 50 % флегматизатора; перекись бензоила и цик-логексанона ( 30 % флегматизатора); перекиси лауроила и дику-мила, гидроперекиси тетралина и пинана, перекись ацетила ( 75 % флегматизатора); гидроперекись трет-бутила без флегматизатора и подобные вещества допускается перевозить в сосудах, оцинкованных горячим способом. [28]
С другой стороны, исследования, проведенные в кашей лаборатории 1 ще в 1938 г. [6], показали, что некоторые вещества, известные как активные замедлители окисления нефтяных масел ( фенил - - нафтил-амнн, гидрохинон, резорцин, ос-нафтол, п-оксидифениламин), не обнаруживают сколько-нибудь значительного и отчетливо выраженного в одном определенном направлении действия на термический распад гидроперекиси тетралина, либо совсем не влияют на него, но чрезвычайно активно тормозят первоначальное образование этой гидроперекиси при автоокислоппи тетралина при низкой температуре, при которой гидроперекись устойчива. Из этих наблюдений был сделан вывод, что исследованные замедлители автоокисления углеводородов действуют скорее на реакцию первичного возникновения гидроперекисей ( в индукционном периоде), чем на распад уже образовавшихся гидроперекисей в ходе дальнейшего развития реакции. Предположения, чго замедлители влияют на окислительный процесс в стадии его инициирования, высказываются в последнее время все чаще. [29]
При автоокислении алкильных боковых цепей в ароматических углеводородах атака происходит по метиновой или метиленовой группе, связанной с циклом. Таким образом получаются гидроперекиси тетралина, этилбензола, - ксилола, кумола, дифенилметана, индана и октагидроан-трацена. [30]
Страницы: 1 2 3 4