Чистая гидроперекись
Cтраница 3
Используя аналогичные условия, но удлиняя время реакции до 150 ч, Караш и Барт11 получили 1 2 % чистой гидроперекиси. [31]
Однако наряду с цитированными выше работами в литературе опубликованы результаты еще двух исследований, первое [12] из которых посвящено изучению термического разложения чистой гидроперекиси кумола, а также в смеси ее с кумолом и хлорбензолом; второе же исследование [13] посвящено изучению той же реакции в 5 и 30 % - ном растворах гидроперекиси кумола в кумоле. [32]
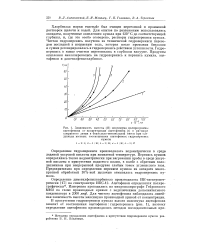
С этой целью были поставлены параллельные опыты окисления метилциклогексана в чистом виде и с добавкой 1 % сырой перекиси метилциклогексана ( содержащей 65 % чистой гидроперекиси) при 80 в течение 128 час. Окисление осуществлялось путем барботирования углеводорода кислородом со скоростью 1 мл / мин в удлиненных кварцевых сосудах ( загрузка 20 г) с пришлифованными к ним стеклянными обратными холодильниками ( фиг. [33]
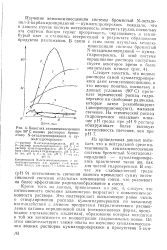 |
Кинетика хемилюминесценцйи при 90 С водных растворов бромистого N-октадецилпиридиния и ку-мил гидроперекиси. [34] |
Из приведенных данных вытекает, что в нейтральной среде интенсивность хемилюминесценцйи системы бромистый М - октадецил-пирндиний - кумилгидроперекись практически такая же, как для чистой гидроперекиси. [35]
Взаимодействие алкильных гидроперекисей с водными растворами гидроокиси натрия было широко использовано для выделения из реакционной смеси гидроперекисей в виде их солей, которые затем в водном растворе подвергали обработке двуокисью углерода с целью получения чистых гидроперекисей. [36]
Авторы окисляли н-гептан при ультрафиолетовом облучении ( 80) и перегонкой при 0 08 мм рт. ст. выделили небольшие количества получающейся при этом гидроперекиси. Обработкой чистой гидроперекиси 10 % - ным раствором едкого натра на масляной бале при 110 из нее получили около 70 % гептана и 30 % гептанола. [37]
Установлено, что в чистой гидроперекиси и в ее концентрированных растворах все гидроксильные группы входят в образованные водородными связями комплексы, которые диссоциируют при разбавлении. [38]
Очистка этой гидроперекиси сопряжена с большими трудностями, так как она разрушается в процессе щелочной экстракции ( с образованием полимера, а-нафтола, 1 4-дигидронафтола и кислот), а перегонка сырого продукта не дает желаемого результата. Однако завершающая перегонка продукта, сконцентрированного с помощью селективной экстракции, позволяет получить небольшое количество относительно чистой гидроперекиси. Тем не менее, даже столь чистое вещество способно по-лимеризоваться при хранении. [39]
Химический метод основан на способности гидроперекиси образовывать с растворами едкого натра натриевую соль, из которой затем выделяют чистую гидроперекись. [40]
Хлорбензол марки чистый был очищен перегонкой и промывкой раствором щелочи и водой. Для опытов по разложению использовались оксидаты, полученные окислением кумола при 120 С до соответствующей глубины, и, где это особо оговорено, растворы гидроперекиси кумола. Чистая гидроперекись получена из технической гидроперекиси переводом последней в натриевую соль, которая после промывки бензолом и сушки регенерировалась в гидроперекись действием углекислоты. [42]
В ранних работах изучались кинетика117 и продукты реакции118 разложения гидроперекиси кумола в растворителях и была подтверждена радикальная природа реакций. Парофазный пиролиз чистой гидроперекиси при 200 - 220 С дал главным образом ацетофенон наряду с относительно небольшими количествами формальдегида, фенола, диметилфенилкарбинрла и а-метилстирола. Хотя газообразные продукты в этом случае не исследовались и, следовательно, присутствие метана и этана не могло быть подтверждено, весьма вероятно, что небольшое количество формальдегида образовалось за счет присутствующих в процессе метальных радикалов. [43]
Всестороннее изучение термического разложения гидроперекиси кумола в ряде растворителей выполнено Карашем, Фоно и Нуденбергомш. Ими установлено, что в предельных углеводородах гидроперекись устойчива до 130 - 140 С, тогда как 48-часовое нагревание в кумоле при 128 С вызывает полное ее разложение. Такая стабильность согласуется с результатами упоминавшихся ранее исследований чистых гидроперекисей, но противоречит данным Фордама и Вильямса 6, которые сообщили о полном разложении гидроперекиси в кумоле за 2 ч при 100 С. [44]
Выделение гидроперекиси из оксидата проводилось через натриевую соль, которая получалась взаимодействием эквимолекулярного количества раствора едкого натра ( 40 % - ного) с разбавлением в бензоле ( 1: 1) оксидатом при охлаждении до 5 С. Чистая гидроперекись представляет собой прозрачную жидкость со следующими характеристиками: d420 1 1929; я / 0 1 5389; MR 48 99 ( вычисл. [45]
Страницы: 1 2 3 4