Образовавшаяся гидроперекись
Cтраница 3
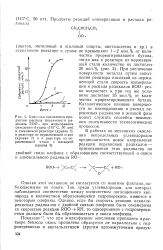
Если считать, что кислород в реакции потребляется полностью ( в смесях с недостатком его), то очевидно, что количество образовавшейся гидроперекиси больше в том случае, когда начальное давление кислорода больше. Известно [59], что при распаде гидроперекисей наблюдается хемилюминесценция. [31]
 |
Схема установки для окисления изопропилбензола до гидроперекиси. [32] |
При окислении изопропилбензола необходимо следить за температурой, которая не должна быть выше 118 С ( при 120 С начинается термический распад образовавшейся гидроперекиси), и расходом воздуха, так как при повышении расхода увеличивается унос изопропилбензола из реактора, что вызывает повышение рН и ведет к значительному распаду гидроперекиси изопропилбензола. [33]
Способность гидроперекисей к перегруппировкам с образованием перекисных соединений иного типа должна быть также принята во внимание при учете возможных направлений превращений первично образовавшихся гидроперекисей в ходе окислительного процесса. [34]
Реакция идет с автоускорением. В начале реакции количество образовавшейся гидроперекиси практически совпадает с количеством поглощенного кислорода. [35]
Изменение значения показателя преломления лежит в основе расчета количества образующихся продуктов распада. Кроме того, необходимо знать количество образовавшейся гидроперекиси, которое определяют иодометрическим методом. [36]
По мнению некоторых исследователей [6], различные антиокислители, активно тормозящие цепную реакцию автоокисления в период ее зарождения, неодинаково влияют на окислительный процесс в стадии его развития. В то же время ионол практически не способен разлагать уже образовавшиеся гидроперекиси и не обладает способностью связывать в комплексы ионы металлов переменной валентности. В ряде случаев, например в целях стабилизации пищевых концентратов и витаминов, ионол применяется ограниченно вследствие нерастворимости в воде. [37]
В настоящее время в литературе имеется большое число работ по использованию полярографических измерений в неводных средах для количественных исследований процессов окисления. Так, например, в работе по окислению парафина [27] анализ образовавшихся гидроперекисей производили полярографически. [38]
Так, среди углеводородов, для которых наблюдается соответствие между количеством поглощенного кислорода и количеством образовавшейся гидроперекиси, имеются и некоторые олефины. Однако, если бы скорость реакции алкилпе-рекисных радикалов с двойной связью олефинов была соизмерима со скоростью реакции ROO - RH, то одновременно с гидроперекисями должны были бы образовываться и окиси олефинов. [40]
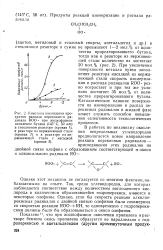 |
Кинетика накопления про - может служить способом повыше. [41] |
Так, среди углеводородов, для которых наблюдается соответствие между количеством поглощенного кислорода и количеством образовавшейся гидроперекиси, имеются и некоторые олефины. [42]
Разрушение полимеров, вызванное окислением, как указывалось выше, связано с образованием в первую очередь гидропе-рекисных соединений, способных к разложению с разрывом С-С - связей. В этом случае применение ингибиторов типа антиоксидантов предотвращает дальнейшее развитие цепного процесса окисления и при употреблении соответствующих препаратов обезвреживает образовавшиеся гидроперекиси путем химического взаимодействия с ними. [43]
В этих условиях в реакции, как правило, образуется набор продуктов окисления, многие из которых подвергаются дальнейшим превращениям, и кинетика реакции очень сложна [108, 141-149], При достаточно низких температурах в результате цепной реакции образуется в основном гидроперекись [146, 150 - 156], которая в этих условиях достаточно устойчива и не подвергается дальнейшим превращениям. При применении фотохимического инициирования или специальных инициаторов - веществ, распадающихся на радикалы, - легко удается обеспечить скорость зарождения цепей значительно большую скорости распада образовавшейся гидроперекиси на радикалы. При этом реакция окисления становится неразветвленной, и ее кинетика оказывается несравненно проще. [44]
Алкоксигруппы значительно труднее замещаются на перекисную группировку, чем атомы галоидов в галоидсиланах. При - действии Н2О2 на ( СНз) 2 ( С6Н5) 51С1 в ледяной уксусной кислоте получается фенол, что связано, очевидно, с перегруппировкой промежуточно образовавшейся гидроперекиси. Для перекисей C6H5) 3Si - ОО - С ( СН3) з и ( СНзЫС6Н5) 51 - ОО - С ( СН3) з перегруппировки не наблюдается. ОО - С ( СН3) з; она медленно гидролизуется водой ( быстрее в присутствии кислот) с образованием грег-бутилгидроперекиси. В нонане эта перекись термически устойчива и разлагается при температуре выше 140 С. [45]
Страницы: 1 2 3 4