Гиншельвуда
Cтраница 2
В целом о схеме Кюллиса и Гиншельвуда может быть сделано то же замечание, какое было обращено и в адрес схем Уолта. Действительно, в конце 40 - х годов без экспериментального решения вопроса о первичном молекулярном продукте п о природе вещества, обусловливающего разветвление, любой механизм, предлагаемый на основе косвенных доказательств, носил спекулятивный характер. [16]
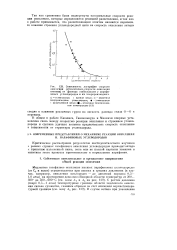 |
Зависимость логарифма скорости окисления ( относительно скорости окисления пентана от фактора стабильности у парафиновых углеводородов и их хлорпроизводных. [17] |
В общем в работе Кюллиса, Гиншельвуда и Малкахи впервые установлена связь между скоростью реакции окисления и строением углеводорода и сделана удачная попытка предвычислитъ скорость окисления в зависимости от структуры углеводорода. [18]
На основе экспериментальных данных Томпсона и Гиншельвуда [2] и Ленера [4], в 1937 г. Лыоис и Эльбе [5] предложили радикально-цепную схему окисления этилена. В этой схеме отвергается часто встречающееся в среде химиков-органиков представление о присоединении кислорода по двойной связи олефиновой молекулы. [19]
Под влиянием работ школ Семенова и Гиншельвуда появилось большое число исследований механизма окисления органических соединений в газовой и жидкой фазах. Вскоре была сформулирована основная задача исследований в этой области - определение констант элементарных реакций сложного радикально-цепного процесса окисления с целью рассчитать скорость реакции окисления по ее гипотетическому механизму. [20]
Критическая энергия разложения, рассчитанная по Гиншельвуду, оказалась равной 37 4 ккал / моль. [21]
 |
Зависимость константы скорости разложения азометана от его начального давления. [22] |
Это совпадает с требованием теории Линде-мана - Гиншельвуда, но в общем не соответствует данным опыта. [23]
 |
Зависимость времени прохождения холодных пламен от начального давления смеси ( 50 / 0-ная смесь диэтилового эфира с кислородом, Т 108 С. [24] |
В 1947 г. появилась работа Кюллиса и Гиншельвуда [50], в которой изучалось нижнетемпературное окисление пентана и гексана в статических условиях в кварцевом реакционном сосуде. [25]
Это со1впадает с требованием теории Линдемана - Гиншельвуда, но в общем не соответствует данным опыта. [26]
Кроме того, если из данных Вильбурна и Гиншельвуда вычислить предэкспоненциальный множитель для константы скорости реакции ( 0), то получается величина порядка 10 - 19 см3 / сек, хотя, как известно, обычные значения предэкспонентов бимолекулярных реакций порядка 10 - 10 см3 / сек. [27]
 |
Изменение константы скорости изомеризации циклопропана с давлением. [28] |
Таким образом и получается, что теория Линдемана - Гиншельвуда предсказывает одинаковую форму ( но не одинаковое положение) кривых gklkm / ( Igp) для всех молекул, как бы сложны они ни были. [29]
В первом параграфе настоящей главы разбираются работы Уолша м Гиншельвуда, во втором - работы В. Я. Штерна и в третьем - работы Норриша. [30]
Страницы: 1 2 3 4