Гиншельвуда
Cтраница 3
Механизм реакции Бухерера явился предметом недавних кинетических исследований Коудри и Гиншельвуда. Реакция нафтио-новой кислоты и кислоты Лорана с HSO3 - бимолекулярна. Предполагаемый механизм включает 1 2-присоединение HSO - к двойной связи, соседней с аминогруппой. Эта стадия определяет скорость реакции. Конечными продуктами гидролиза являются соответствую - щие нафтолы. Влияние изменения рН на скорость реакции указывает на наличие двух отрицательных ионов - НЗО и CioH6 ( NH2) SO. Были выделены также промежуточные продукты реакции присоединения HSO к нафтионовой кислоте. Главным продуктом является, по всей вероятности, димер дибисульфита. Реакция между 1-нафтол - 4 - или 5-сульфонатами и HSO -, ведущая к образованию соответствующего бисульфитного комплекса, обратима. Прямая реакция - бимолекулярная, а диссоциация комплекса - мономолекулярная реакция. [31]
Близкие к единице значения величины Р, согласно расчетам Вилль-бурна и Гиншельвуда [1294], а также В. В. Воеводского и А. Б. Налбан-дяна [203], получаются также в случае присоединения атома Н к молекуле Оа, когда третьей частицей является двухатомная молекула. При М СО2 и Н2О величина Р оказывается больше единицы зэ. [32]
Однако, как показал В. В. Воеводский [64], точка зрения Вильбурна и Гиншельвуда неверна. [33]
При рассмотрении же экспериментальных результатов, полученных в смесях, содержащих пары воды, Вильбурну и Гиншельвуду приходится прибегать к туманному упоминанию о действии воды, адсорбированной на стенке, что в их условиях не имеет смысла, так как весь расчет основан на предположении о диффузионной области протекания реакции ( 7), из чего следует, что / С7 не зависит от eHOl и, следовательно, от адсорбции воды. Кривая / на рис. 50 изображает экспериментальные данные Вильбурна и Гиншельвуда о зависимости скорости реакции от парциального давления водорода при ро, 200 мм рт. ст. и 570 в сухой смеси, кривая 2-в таких же смесях с парциальным давлением паров воды 11 мм рт. ст. Кривая 3 представляет собой результат точного теоретического расчета Вильбурна и Гиншельвуда для кривой 2, исходя из констант, полученных при анализе других данных по медленному окислению. [34]
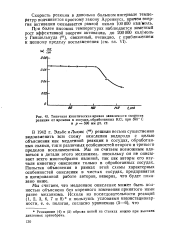 |
Типичная кинетическая кривая зависимости скорости. [35] |
При более высоких температурах наблюдается заметный рост эффективной энергии активации, до 200000 кал / моль у Гиншельвуда ( 67), связанный, очевидно, с приближением к цепному пределу воспламенения ( см. гл. [36]
Если разложение N2O должно протекать в условиях, наиболее благоприятных в отношении активации, то в качестве катализатора следует взять металл, обладающий средним по величине значением работы выхода. Согласно данным Гиншельвуда и Причарда [69], энергия активации на золоте ( Ф 4 71 в) равна 29 0 ккал, а на платине ( Ф 5 36 в) 32 5 ккал. [37]
По мнению Гранта и Гиншельвуда ( 1933 г.), реакции между молекулами и ионами протекают нормально. Большинство из упоминавшихся выше реакций с участием алкоголятов натрия попадают в категорию нормальных, если считать, что в растворе алкоголя. Реакции между галоидными этилами и едким кали в растворе в этиловом спирте, при которых одним из реагирующих веществ является ион, также идут с нормальными скоростями, близкими к вычисленным величинам. Некоторые расхождения между вычисленными и наблюдаемыми константами скорости могут быть отнесены за счет ошибок в определении числа столкновений, так как формула для числа столкновений в газе, несомненно, применима лишь приближенно в том случае, когда одна из сталкивающихся частиц представляет собой ион. Использованные в этой формуле величины энергии активации со всей точностью неизвестны, что также может привести к ошибкам. [38]
Стиси и соавтор ( 140) показали, что добавка окиси азота не уничтожает полностью реакционных цепей, но лишь резко уменьшает их длину. Поэтому вычисляемая по Стевли и Гиншельвуду средняя длина реакционной цепи имеет обычно пониженное значение. [39]
При рассмотрении же экспериментальных результатов, полученных в смесях, содержащих пары воды, Вильбурну и Гиншельвуду приходится прибегать к туманному упоминанию о действии воды, адсорбированной на стенке, что в их условиях не имеет смысла, так как весь расчет основан на предположении о диффузионной области протекания реакции ( 7), из чего следует, что / С7 не зависит от eHOl и, следовательно, от адсорбции воды. Кривая / на рис. 50 изображает экспериментальные данные Вильбурна и Гиншельвуда о зависимости скорости реакции от парциального давления водорода при ро, 200 мм рт. ст. и 570 в сухой смеси, кривая 2-в таких же смесях с парциальным давлением паров воды 11 мм рт. ст. Кривая 3 представляет собой результат точного теоретического расчета Вильбурна и Гиншельвуда для кривой 2, исходя из констант, полученных при анализе других данных по медленному окислению. [40]
В указанный промежуток времени были предложены четыре радикально-цепных схемы окисления высших парафиновых углеводородов. Из них первые две - Уолша ( 1946 - 1947) и Гиншельвуда ( 1947) - являются перекисными схемами в том смысле, что в них, во-первых, принимается образование органических перекисей в качестве первичных молекулярных продуктов окисления и, во-вторых, именно этим перекисям приписывается разветвляющая роль. [41]
Большое значение приобрела также теория цепных реакций, начало которой было заложено в работах Н. А. Шилова ( 1904) и которая получила развитие в работах Н. Н. Семенова и Гиншельвуда. [42]
Учет температурной зависимости коэффициента диффузии может несколько повысить эту величину. Однако в ряде случаев при сильном диффузионном торможении возможны существенные отклонения от этого соотношения, как показали Шнейдер и Мичка [655] для реакции, описываемой кинетическим уравнением типа Лэнгмюра - Гиншельвуда. [43]
При рассмотрении же экспериментальных результатов, полученных в смесях, содержащих пары воды, Вильбурну и Гиншельвуду приходится прибегать к туманному упоминанию о действии воды, адсорбированной на стенке, что в их условиях не имеет смысла, так как весь расчет основан на предположении о диффузионной области протекания реакции ( 7), из чего следует, что / С7 не зависит от eHOl и, следовательно, от адсорбции воды. Кривая / на рис. 50 изображает экспериментальные данные Вильбурна и Гиншельвуда о зависимости скорости реакции от парциального давления водорода при ро, 200 мм рт. ст. и 570 в сухой смеси, кривая 2-в таких же смесях с парциальным давлением паров воды 11 мм рт. ст. Кривая 3 представляет собой результат точного теоретического расчета Вильбурна и Гиншельвуда для кривой 2, исходя из констант, полученных при анализе других данных по медленному окислению. [44]
При низких давлениях эта реакция не идет как цепная из-за того, что активные частицы - атомы кислорода - гибнут на стенках сосуда и не образуют цепи. При повышении давления диффузия атомов кислорода к стенкам затрудняется, и в объеме возникает цепная реакция, сопровождающаяся холодным пламенем. Гиншельвуда к открытию нового явления, заключающегося в существовании двух пределов воспламенения - нижнего и верхнего. При низких давлениях активные частицы ( например, атомы О) сравнительно часто достигают стенок сосуда и гибнут на них. [45]
Страницы: 1 2 3 4