Глим
Cтраница 1
Глим - 1) употребляемое в химии название 1 2-диметоксиэтана СН3ОСН2СН2ОСН3; 2) фупповое название соединений, простейшим из которых является 1 2-диметоксиэтан; отвечают общей формуле СН3 ( ОСН2СН20) д - СН3; при п 2 соединение называется диглим. [1]
Хотя глим комплексуется только с катионом, строение аниона может оказывать сильное влияние на константу комплексо-образования, особенно если изменение в строении аниона является результатом изменения состояния сольватации ионной пары. [2]
Токсичность глимов при приеме внутрь не растет пропорционально при повторном введении; их токсичность выше, чем гликолей. [3]
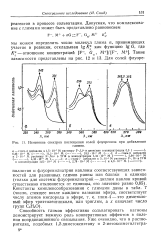 |
Изменение спектров поглощения солей флуоренила при добавлении. [4] |
Способность глимов эффективно сольватировать катионы демонстрирует важную роль кооперативных эффектов в явлении координационного связывания. [5]
ДМСО, глим, гексан и эфир. В большинстве случаев наилучшие выходы кислот получают при проведении реакции в течение нескольких часов при комнатной температуре. [6]
СНз ( глимы) - чрезвычайно эффективные сольватирующие агенты по отношению к катионам щелочных металлов; они часто используются для усиления реакционной способности органических соединений щелочных металлов. Их способность вступать в координационную связь с ионами щелочных металлов зависит от числа соответствующих координирующих мест. Мы обсуждаем эти системы подробно, поскольку их комплексообра-зование с солями флуоренила обнаруживает ряд интересных особенностей, что облегчает понимание процесса сольватации ионной пары. Еще более эффективны по сравнению с линейными глимами макроциклические эфиры, которые подробно будут рассмотрены в разд. [7]
Поэтому эффективность глимов в качестве координирующих агентов главным образом обусловлена меньшей потерей энтропии по сравнению с растворителями типа ТГФ. [8]
Процесс комплексообразования глимов с флуоренилкалием отличается от процесса комплексообразования с натриевой и литиевой солями флуоренила. Как показано на рис. 15, зависимость lg / С от lg [ G ] заметно отклоняется от прямой. Отношение [ F-G K ] / [ F-K ] для глима-6 и глима-7, вероятно, достигает постоянного значения при более высоких концентрациях глима. [9]
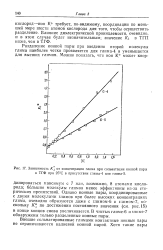 |
Зависимость / с от концентрации глима при сольватации ионной пары в ТГФ при 25 С в присутствии глима-4 или глима-5. [10] |
Внешне сольватированные глимами контактные ионные пары не ограничиваются калиевой ионной парой. [11]
Кроме того, глим относительно летуч, легко отделяется от продукта, не имеет достаточно кислых атомов водорода, которые могли бы обмениваться с енолят-анионами, и за счет сольватирования повышает реакционную способность анионов. [12]
Для высоких концентраций глима, как, например, в системах с глимом-4 или глимом-5, допустимо принять, что / Ci [ G ] l, т.е. все контактные ионные пары внешне сольватированы глимами. [13]
В зависимости от содержания глима в инертной или менее соль-ватирующей, чем глим, среде в разных количествах будут образовываться комплексы 1: 1, или 1: 2, или оба комплекса одновременно. Образование более сольватированных частиц сопровождается увеличением теплоты и уменьшением энтропии компле-ксообразования. [14]
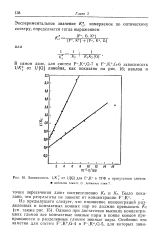 |
Зависимость / К от 1 / [ Q ] для F. K 1 в ТГФ в присутствии глимов. [15] |
Страницы: 1 2 3 4