Глим
Cтраница 2
Однако при достаточно высоких концентрациях глимов все контактные ионные пары в конце концов превращаются в разделенные глимом ионные пары. [16]
Рыхлые ионные пары, разделенные глимом и ТГФ, имеют один и тот же максимум поглощения. [17]
Трихлорацетат натрия отщепляет СО2 в глиме при 80 С. В МФК-реакциях в неполярных растворителях сухой трихлор-ацетат аммония разлагается медленно даже при комнатной температуре. [18]
Это неудивительно для растворов в глимах, поскольку в этих растворителях дианионы трифенилбензола, по всей вероятности, находятся в виде свободных ионов. Однако в чистом метилтетрагидрофуране или его смесях с глимами дианион трифенилбензола должен испытывать сильное возмущающее влияние со стороны катионов. Увеличение параметра D в растворителях низкой полярности по сравнению с глимами и зависимость параметра D от природы катиона подтверждают образование ионных пар. [19]
Чтобы избежать образования пероксидов в глиме, последний пропускали через колонку с активированным оксидом алюминия. Очищенный таким образом глим хранили над оксидом алюминия. [20]
Разделение ионной пары при введении второй молекулы глима наиболее четко проявляется для глима-4 и уменьшается для высших глимов. [21]
Первая реакция имеет место даже в отсутствие глима. [22]
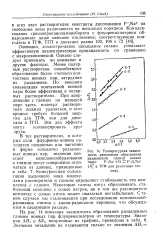 |
Температурная зависимость равновесия образования. [23] |
На рис. 14 показана зависимость образования разделенных глимом ионных пар флуоренилнатрия от температуры. [24]
Однако ионные пары, координированные с двумя молекулами глимов при более высоких концентрациях глима, очевидно образуются даже с глимом-6 и глимом-7, поскольку К по достижении постоянного значения ( см. рис. 15) в конце концов снова увеличивается. В чистых глиме-6 иглиме-7 обнаружены только разделенные ионные пары. [25]
Первые две соли дают сильные парамагнитные сдвиги протонов глима в слабое поле, а третья - диамагнитный сдвиг в сильное поле. [26]
ЛДЮ дибензо-18 - краун-6 при приеме внутрь меньше ЛДЮ глима, этиленгликоля и моноэфира этиленгликоля. Известно, что биологическая активность и токсичность веществ могут быть существенно изменены за счет изменения заместителей, так что следует продолжить исследования токсичности модифицированных производных краун-эфиров, чтобы найти среди них малотоксичные. [27]
Комплексообразование макроциклических эфиров с ионными парами флуоренила напоминает поведение глимов. Добавление дибензо - или дициклогексил-18 - крауна-6 к флуоренилнатрию в ТГФ или ТГП приводит к образованию комплекса 1: 1 с максимумом поглощения 372 нм. [28]
Это согласуется с результатами, полученными для флуоренилнатрия в смесях глимов и ТГФ; однако следует подчеркнуть, что метод, основанный на изучении равновесия контактная ионная пара - сольватно разделенная ионная пара, дает разницу в состоянии сольватации между двумя видами ионных пар, в то время как изучение равновесия в системе би-фенил - натрий позволяет определить общее число молекул глима, связанных с ионной парой. [29]
В зависимости от содержания глима в инертной или менее соль-ватирующей, чем глим, среде в разных количествах будут образовываться комплексы 1: 1, или 1: 2, или оба комплекса одновременно. Образование более сольватированных частиц сопровождается увеличением теплоты и уменьшением энтропии компле-ксообразования. [30]
Страницы: 1 2 3 4