Диффузия - ион - железо
Cтраница 2
Второй, более рыхлый слой магнетита образуется преимущественно из-за диффузии ионов железа в воду. Диффузионные потоки ионов железа в воду и кислорода к металлу из воды через слой оксидов почти равновелики. Ионы железа, проникающие в воду, после реакции с ионами кислорода оседают на стенки трубы в виде кристаллов рыхлого слоя магнетита. Возможно, что часть этих кристаллов уносится потоком воды или пароводяной смеси. [16]
Окисная пленка на поверхности корродирующего металла образуется за счет диффузии ионов железа через магнетит. На границе раздела окисла и воды ион железа реагирует с гидроксилом или молекулой воды и образует гидрат закиси железа, в итоге образуется магнетит. В воде при температуре 300 С за счет взаимодействия с железом гидрат окиси железа также переходит в магнетит. С течением времени толщина окисной пленки увеличивается, а диффузия ионов железа через нее затрудняется. Это обстоятельство ведет к уменьшению скорости коррозии - во времени. [17]
В настоящее время считается, что при окислении железа определяющими факторами являются диффузия ионов железа в слоях вюстита и магнетита и диффузия ионов кислорода в слое гематита. [18]
При образовании FeO на границе металл - покрытие ограничивающим фактором является скорость диффузии ионов железа через слой окислов. Регулировать этот процесс можно, применяя бескислородные или трудноотдающие кислород покрытия. [19]
 |
Структура защитного слоя магнетита в результате воздействия па перлитную сталь при 300 С. [20] |
В результате же воздействия раствора гидразина размеры кристаллов резко уменьшаются, что затрудняет диффузию ионов железа в рабочую среду и снижает интенсивность протекающей коррозии. В еще большей мере это проявляется при комплексонной обработке, для которой характерно не только еще большее уменьшение величины кристаллов магнетита, но и неправильная их форма, способствующая их наиболее плотной упаковке, с наиболее высокими защитными свойствами. [21]
При протекании реакции окисления в диффузионной области возможны также механизмы, включающие, например, стадию диффузии ионов железа по вакантным узлам решетки. [22]
Таким образом, новая ( о) модификация гематита, вследствие своей дырчатости и ослабленное связей, сильно облегчает диффузию ионов железа и ускоряет процесс окисления. Усиленный поток этих ионов к наружной поверхности окалины приводит к изменению ее текстуры. Она повышает степень совершенства и становится текстурой свободного роста. Таким образом, примерно до 800 С ведущей стадией процесса является диффузия кислорода, а при более высоких температурах рост окалины обусловлен в основном диффузией железа. [23]
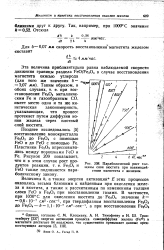 |
Параболический рост толщины слоя вюстита при взаимодействии магнетита с железом. [24] |
Ре и газообразным СО, имеет место одна и та же кинетическая закономерность, указывающая, что процесс протекает путем диффузии ионов железа через плотный слой вюстита. [25]
Однако сомнительно, чтобы наблюдение Энгелла и Вефера о глубоком внедрении индикаторов в слой вюстита свидетельствовало о диффузии кислорода в дополнение к диффузии ионов железа. Как установили Данингтон, Бек и Фонтана [347], образующиеся в вюстите вакансии способны диффундировать через листовое железо, так что одна из поверхностей раздела может выполнять роль поглотителя вакансий, образующихся по обе стороны окисляющегося листа. Таким образом, вещество в вюстите переносится, бесспорно, катионами. [26]
Окисление железа парами воды подчиняется экспоненциальному закону, описываемому уравнением Аррениуса, в связи с чем лимитирующей стадией процесса восстановления окиси железа является скорость диффузии ионов железа и встречной диффузии ионов кислорода в твердой фазе. [27]
Следовательно, скорость реакции взаимодействия подчиняется параболической закономерности. Тот факт, что скорость диффузии ионов железа в FeS гораздо больше скорости диффузии серы, подтвердили Кондит и Бнрче-нолл в 1961 г. путем измерения собственной диффузии с помощью меченых атомов. [28]
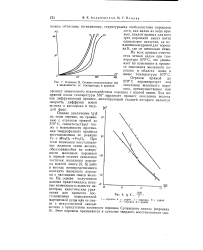 |
Порошок В. Степень использования ( т в зависимости, от температуры и времени. [29] |
С характеризует ход окисления железного порошка, преимущественно как процесс химического взаимодействия порошка с влагой окиси. Ход же прямой после температуры 570 выражает процесс окисления железа как диффузионный процесс, лимитирующей стадией которого является скорость диффузии ионов железа и кислорода в твер - л дои фазе. [30]
Страницы: 1 2 3 4