Полярная гидрофильная группа
Cтраница 1
Полярные гидрофильные группы в глобуле расположены на ее внешней поверхности, а неполярные гидрофобные группы обращены внутрь глобулы. Благодаря этому наружная поверхность белка гидратируется, что повышает растворимость белка и обусловливает возможность его участия в биохимических реакциях, которые в физиологических условиях протекают в водной среде. [1]
В роли полярных гидрофильных групп в молекулах органических соединений обычно выступают группы: NH2, ОН, SH, СООН, SO3H и др., а в роли неполярных групп - углеводородные цепи или циклы. [2]
В роли полярных гидрофильных групп в молекулах органических соединений обычно выступают группы: NH2, ОН, SH, СООН, ЗОзН и др., а в роли неполярных групп - углеводородные цепи или циклы. [3]
В качестве полярных гидрофильных групп при синтезе ПАВ используют анионы сульфогрупп и кислых эфиров серной и фосфорной кислит, карбоксильные, фенольные и аминогруппы либо спиртовые, окисные и полиэфирные. В соответствии с этим все ПАВ подразделяются на ионогенные и неионогенные. [4]
Такая структура характеризуется накоплением полярных гидрофильных групп на одном конце молекулы и образованием двух длинных углеводородных хвостов, состоящих из остатков жирных кислот. Эти хвосты образуют гидрофобную область и группы молекул фосфо-липидов, подходящим образом ориентированных, естественно, создают определенную гетерогенность в растворе. [5]
 |
Строение мицеллы. Гидрофобные хвосты обращены внутрь частицы. [6] |
Структура фосфоли-пида характеризуется накоплением полярных гидрофильных групп на одном конце молекулы и образованием двух длинных углеводородных хвостов, состоящих из остатков жирных кислот. [7]
Глюкоза является доступным и удобным источником полярных гидрофильных групп при синтезе поверхностноактивных веществ. Один из способов ее использования для этой цели заключается в применении легко синтезируемых и относительно устойчивых глюкозидов. Метилглюкозид, например, получают путем переэтерификации сложными эфирами жирных кислот, включая глицериды [73], но продукты этой реакции ограниченно растворимы в воде. [8]
Молекулы обычных ПАВ имеют асимметричное строение и содержат полярные гидрофильные группы, имеющие сродство к воде, и углеводородные гидрофобные радикалы, имеющие сродство к углеводородам. В поверхностном слое, например на границе раздела нефть-вода, молекулы ПАВ ориентированы так, что полярная часть обращена к воде, а гидрофобная к нефти. [9]
Очевидно, активность поверхностных сил тем выше, чем меньше полярная гидрофильная группа молекул и длиннее углеводородная цепь. [10]
В этом случае наружная поверхность коллоидных частиц всегда покрыта полярными гидрофильными группами. Эти группы гидратируют-ся водной средой, что обеспечивает устойчивость и самопроизвольное образование мицелл. [11]
В противоположность белкам молекулы дезоксирибонуклеиновой кислоты, которые содержат большое число полярных гидрофильных групп, на границе воздух - вода располагаются также горизонтально, но не развертываются. [12]
Растворимость белка зависит от отношения числа неполярных гидрофобных групп к числу полярных гидрофильных групп в молекуле, от их взаимного расположения и от результирующего дипольного момента. Заряженные полярные группы электростатически взаимодействуют друг с другом как внутри одной и той же молекулы, так и межмолекулярно, однако в воде эти силы благодаря высокой диэлектрической постоянной убывают и возникает повышающее растворимость взаимодействие между полярными группами и молекулами воды. Альбумины и псевдоглобулины очень легко растворимы в воде, так как в этом случае взаимодействие между белком и растворителем сильнее, чем взаимодействие между соседними молекулами белка. Эвгло-булины в воде нерастворимы, поскольку здесь более сильным является взаимодействие между молекулами белка. Добавление к воде такого растворителя как этиловый спирт снижает диэлектрическую постоянную и вместе с тем приводит к замене части молекул воды. Благодаря этому белки, очень хорошо растворимые в воде, в водно-спиртовых смесях растворяются гораздо хуже. Например, растворимость яичного альбумина или карбо-ксигемоглобина лошади [193] в 25 % - ном этиловом спирте при - 5 составляет всего лишь небольшую долю их растворимости в воде. При таких концентрациях этилового спирта денатурацию предотвращают хранением раствора при возможно более низкой температуре. [13]
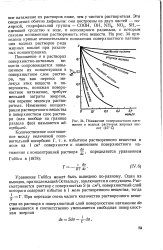 |
Понижение поверхностного натяжения в водных растворах жирных кислот ( 15 С. [14] |
Эти соединения обычно дифильны: они построены из двух частей - полярной, гидрофильной группы - СООН, ОН, NH2, NO2, SH - имеющей сродство к воде, и неполярного радикала, с которым связана пониженная растворимость этих веществ: На рис. 34 приведены кривые относительного понижения поверхностного натяжения водных растворов ряда жирных кислот при различных концентрациях. [15]
Страницы: 1 2 3 4