Другая алкильная группа
Cтраница 1
Другие алкильные группы в положениях 2 6 менее активны, чем метильная. [1]
Гиперконъюгация других алкильных групп по сравнению с ме-тильной понижается, так как уменьшается число связей С - Н; так, связанный с сопряженной системой углерод грег-бутильной группы не имеет ни одной С - Н - связи, поэтому применительно к эффекту Бейкера - Натана метил оказывается наиболее сильным, а трег-бутил - наиболее слабым донором электронов. [2]
В случае других алкильных групп, гидроксильной и карбоксильной групп не найдено простой связи замещения со скоростью гидрогенизации. [3]
Замена метила ка другие алкильные группы R G-положе-нии хинолинового цикла не ведет к альтернированию физиологической активности. [4]
Интересно отметить, что метальные и другие алкильные группы составляют около 50 % алифатического углерода, в лигнитах содержатся более длинные алкильные группы. Авторы считают, что в битуминозных углях количество гидроароматических структур незначительно и их содержание ( как и длинных алкильных цепей) в составе ароматических фракций и в асфальтенах с жесткостью процесса снижается. [5]
Удаление метильных и, по-видимому, других алкильных групп наилучшим образом может быть проведено действием трифторида бора, хотя оно идет неизбирательно и, кроме того, с расщеплением ацегальных и гликозидных связей. Описаны и другие методы 0-деметилирования. [6]
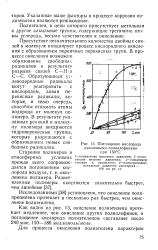 |
Поглощение кислорода. [7] |
Полиэтилен, в цепи которого присутствует метальная и другие алкильные группы, содержащие третичные атомы углерода, весьма чувствителен к окислению. [8]
Это связано с тем, что метальная и другие алкильные группы в большей степени, чем водородный атом, способны компенсировать положительный заряд карбонильного углерода ( стр. Поэтому из перечисленных оксосоединений самым активным в реакциях присоединения является формальдегид. Еще более активен трихлорацетальдегид ( хлораль), поскольку группа СС13 не только не компенсирует положительный заряд углерода карбонильной группы, а, наоборот, оттягивает от него электроны. [9]
Эти данные согласуются с известной электроположительностыо метильной и других алкильных групп ( / - эффект) в карбоновых кислотах; иными словами, алкильные группы намного легче, чем водород, отдают свои электроны электроноакцепторному центру молекулы ( гл. Характер изменения констант диссоциации первых трех гомологов находится в соответствии с рассмотренным ранее ослаблением индуктивного эффекта через простую связь. В то же время следует иметь в виду, что гиперконъюгация должна способствовать значительному увеличению различия между первыми двумя кислотами и незначительному уменьшению различия между следующими кислотами. Влияние поля едва ли может иметь существенное значение в таких молекулах, в которых, помимо самого центра диссоциации, нет полярных заместителей. [10]
Если гидроксил или аминогруппа конкурируют с метальной или другой алкильной группой, или с галоидом, замещение определяется группами - NH2 или - ОН. Диметиламино -, амино - и оксигруппы настолько превосходят все другие орто - и пара-ориентанты, что амины и фенолы подвергаются особым реакциям замещения, неприменимым к другим ароматическим соединениям. Другие орто - и пара-направляющие группы, включенные в приведенный выше перечень, расположены приблизительно в порядке эффективности, судя по конкурентным реакциям, но для групп со сравнительно низкой эффективностью различия относительно малы. Различие между метильной группой и галоидом, например, столь мало, что га-галоидтолуолы обычно образуют смеси двух возможных продуктов замещения. [11]
Если гидроксил или аминогруппа конкурируют с метильной или другой алкильной группой, или с галоидом, замещение определяется группами - NH2 или - ОН. Диметиламино, амино - и оксигруппы настолько превосходят все другие орто - и пара-ориентанты, что амины и фенолы подвергаются особым реакциям замещения, неприменимым к другим ароматическим соединениям. Другие орто - и пара-направляющие группы, включенные в приведенный выше перечень, расположены приблизительно в порядке эффективности, судя по конкурентным реакциям, но для групп со сравнительно низкой эффективностью различия относительно малы. Различие между метильной группой и галоидом, например, столь мало, что и-галоидтолуолы обычно образуют смеси двух возможных продуктов замещения. [12]
Наряду с этиловым эфиром приводятся также соединения с другими алкильными группами, такими, как алкоксиалкильными, циклоалкильными, арильными, аралкильными или алкарильны-ми группами. [13]
В молекулах, в которых метильные группы ( или другие алкильные группы, обладающие связями С - Н) находятся по соседству с двойной связью, тройной связью или бензольным кольцом, наблюдаются некоторые изменения физических и химических свойств. Эти изменения противоположны тем, которые должны были бы произойти. [14]
В молекулах, в которых метильные группы ( или другие алкильные группы, обладающие связями С - Н) находятся по соседству с двойной связью, тройной связью или бензольным кольцом, наблюдаются некоторые изменения физических и химических свойств. Эти изменения противоположны тем, которые должны были бы произойти, если бы алькильные группы обладали исключительно индукционным эффектом. [15]
Страницы: 1 2 3 4