Винильная группа
Cтраница 2
Винильная группа может быть также образована при реакции между адсорбированной молекулой ацетилена и молекулой водорода в физически адсорбированном состоянии. [16]
Винильная группа обладает высокой миграционной способностью в цианоборатной реакции. Гидролиз промежуточных соединений протекает легко и приводит к замещенным аллиламидам определенной стереохимической конфигурации. [17]
Винильные группы оказывают положительное влияние на уменьшение деструкции. [18]
Винильная группа также может стабилизировать карбанионный центр, хотя и не в такой степени, как кетогруппа. [19]
Винильная группа оказывает в большинстве случаев такое же влияние. [20]
Винильная группа может быть определена этим методом в ряде полисилоксанов, за исключением содержащих трифтор-пропильные радикалы, присоединенные к кремнию, так как они при отщеплении также дают этилен. Определению этильных и фенильных групп практически помех нет. [21]
Винильная группа, имеющая помимо - / - эффекта еще и Ч - М - эффект, делает тройную связь даже более реакционно-способной, чем двойная. [22]
Винильная группа, связанная с шестичленным гетероцик-лом, будет иметь иную полярографическую активность, нежели группа, связанная с пятичленным гетероциклом. При этом а-углеродный атом имеет большую электронную плотность, чем находящиеся в - положении по отношению к гете-роатому. Особенности распределения электронной плотности в пятичленных гетероциклах сказываются определенным образом и на полярографической активности винильной группы в их винилзамещенных. При сравнении потенциалов полуволн а-винилфурана и а-винилтиофена видно, что винильная группа в первом восстанавливается труднее, чем во втором. Из эффектов, влияющих на полярографическую активность органических молекул, тут следует учитывать, по крайней мере, два: а) индукционный эффект самого гетероцик-ла, определяющего статическую полярность молекул и, в первую очередь, состояние электронного облака на винильной группе; б) подвижность я-электронной системы в винильном производном, что связано со степенью ароматичности соответствующего гетероцикла, и способность молекул поляризоваться в электрическом поле электрода. [23]
Винильные группы олефинов СН2СН - R, И особенно их разнообразных производных, медленно окисляются кислородом воздуха, который в этом случае вызывает полимеризацию еще не окислившегося непредельного соединения. Окисление протекает по свободнорадикальному механизму. [24]
Обычно винильные группы, расположенные у концов цепи, присоединяют галогеноводород труднее, чем двойные Связи, находящиеся в середине цепи. [25]
Винильная группа стирола также окисляется до формальдегида, но чувствительность определения в этих условиях в три раза ниже по сравнению с определением дивинила. [26]
Отрицательно замещенная винильная группа, например в / 5-ни -, тростироле или в коричной кислоте, ориентирует в орто - н пара-положения. [27]
Поскольку винильная группа в соответствующих производных олова также достаточно лабильна, иногда для синтетических целей вместо дивинилртути используются винильные производные олова. Ввиду токсичности ртутного производного всякий раз, когда это возможно, предпочтительнее пользоваться производными олова. [28]
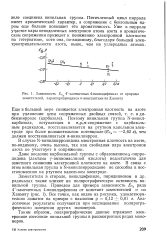 |
Зависимость., 4 -замещенных 4-винилдифенила от природы заместителей, характеризующихся ст-константами по Хаммету. [29] |
Поэтому винильная группа N-винил-карбазола, вступающая в я р зт-сопряжение с карбазоль-ным радикалом, восстанавливается на ртутном капельном электроде при более положительном потенциале ( Е / г - 2 62 в), чем должен восстанавливаться ос-винилпиррол. [30]
Страницы: 1 2 3 4