Гуанидиновая группа
Cтраница 1
Гуанидиновая группа аргинина может блокироваться нитрованием или тозилированием. В случае нитроарги-нина существует опасность расщепления с образованием орнитина. Все еще недостаточно решена проблема защиты цистеина при твердофазном синтезе, хотя перепробовано множество вариантов. Амидные группы глутамина и аспарагина целесообразно защищать. Общеизвестные побочные реакции при применении многофункциональных аминокислот, такие, как, например, транспептидация в случае аспарагиновой кислоты или образование пирролидон-5 - карбоновой-2 кислоты с глутамином, представляют опасность также и в случае синтезов Меррифилда. [1]
Гуанидиновая группа встречается в составе некоторых аминокислот-например, аргинина. [2]
Гуанидиновая группа встречается в составе некоторых аминокислот, например аргинина. [3]
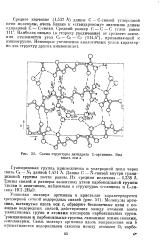 |
Схема структуры дигидрата L-аргинина. Вид вдоль оси а. [4] |
Гуанидиновая группа присоединена к углеродной цепи через связь Св - Ng длиной 1 471 А, Длины С - N-связей внутри гуани-диновой группы почти равны. [5]
Положение гуанидиновой группы доказано частичным синтезом ди-гидро - и изодигидросферофизинов. [6]
Сильноосновные свойства гуанидиновой группы объясняются тем, что про-тонирование иминогруппы ( C NH) приводит к образованию более стабильного катиона, чем протонирование первичной аминогруппы. [7]
Сакагучи на гуанидиновую группу ( Н.А. Серова 1), что, впрочем, не во всех случаях исключает замещение в последней 5 9 g противоположность колхицидил - Z, - орнитину, который образуется из медного соединения L - орнитина, колхицидил - - L - аргинин не получается из соответствующего медного соединения 5, что и является наиболее убедительным доказательством наличия х-замещения в колхицидил - Z, - аргинине. [8]
Интересно отметить, что гуанидиновые группы играют активную роль в осуществлении бактериостатического действия стрептомицина на туберкулезные бациллы. Изъятие гуанидиновых групп ведет к инактивации стрептомицина. [9]
Как уже указывалось, гуанидиновые группы аргинина остаются заряженными при максимально достижимых рН и не дают вклада в кривую титрования. Комбинируя эти данные и учитывая, что число фенольных групп может быть определено путем спектрофотометри-ческого титрования, определяют по отдельности числа всех ионизующихся групп в молекуле белка. Число аминогрупп лизина определяется также путем сравнения кривых титрования, исследованных в обычных условиях и в присутствии формальдегида, взаимодействующего с нейтральной аминогруппой и понижающей значение рК этой группы. [10]
Нитропруссидный метод272 основан на взаимодействии гуанидиновых групп стрептомицина с нитропруссидным реактивом ( окисленный нитропруссид); образующееся окрашенное соединение колориметрируется. [11]
Благодаря наличию в стрептомицине N-метиламинной и двух гуанидиновых групп он является сильным основанием, дающий нейтральные соли с минеральными кислотами. Обычно в медицине применяется сульфат стрептомицина. [12]
Методы модификации остатков аргинина в белках основаны на конденсации гуанидиновой группы с различными дикетонами и диальдегидами. Модификация протекает в мягких условиях ( рН 8 0 - 9 0; 25 - 40 С) в натрий-боратном буфере с образоввнием стабильного комплекса производного аргинина с боратом. [13]
При действии О-метилпсевдомочевины и S-метилпсевдотиомочевины [181] а-аминогруппы аминокислот превращаются в гуанидиновые группы. С [185] и в полиорнитине [ 186а ] также гуанидируются, образуя остатки аргинина. [14]
Эта аминокислота отличается от аргинина лишь тем, что вместо гуанидиновой группы в ней содержится остаток мочевины. Карбонильная группа цитруллина в результате реакции переаминирования, протекающей с участием а-амино-группы аспарагиновой кислоты, превращается в иминогруппу. При этом образуются фумаровая кислота и аргинин, который гидролитически расщепляется ферментом аргиназой на мочевину и орнитин, после чего весь цикл превращений аминокислот начинается сначала. [15]
Страницы: 1 2 3 4