Гуанидиновая группа
Cтраница 2
В другом синтезе ( рис. 39) использовали защищенный лишь по гуанидиновым группам остатков аргинина нонапептид ( В 2 - 10), который в виде соли конденсировали с / г-нитрофени-ловым эфиром а-карбобензокси-е-тозиллизина. [16]
Этим методом было доказано, что в богатых аргинином протаминах сперматозоидов рыб гуанидиновые группы аргинина свободны: они не участвуют в осуществлении связи между аминокислотами. [17]
В стрептомицине три вторичные аминогруппы: две аминогруппы етрептамина входят в состав гуанидиновых групп [ H2N - C ( NH) - NH - ], а одна, входящая в глюкозамин, метилирована. [18]
Примечания, ( а) - терминальные аминогруппы, аминогруппы остатков лизина, гуанидиновые группы остатков аргинина; ( б) - имидазольные группы остатков гистидина, индольные группы остатков триптофана; ( в) - терминальные карбоксильные группы, карбоксильные группы остатков глутаминовой и ас-парагиновой кислот; ( г) - фенольные группы остатков тирозина, гидроксильные группы остатков серина; ( д) - меркаптогруппы остатков цистеина; ( е) - альдегидные группы углеводов. [19]
Аналогичным путем из Na, Ыа-дикарбобензоксиаргинина через N-карбоксиангидрид [2670] получают производное аргинина с защищенной гуанидиновой группой. [20]
Вторичный азот триптофана, пролина и оксипролина, вторичный и третичный азот гистидина, гуанидиновая группа аргинина и. Первичная аминогруппа большинства аминокислот количественно реагирует с азотистой кислотой. Глицинпептиды образуют 120 % от рассчитанного теоретически количества азота. Лизин реагирует с азотистой кислотой а - и е-аминогруппами, причем s - аминогруппа реагирует медленнее. [21]
Моноацильное производное аргинина можно приготовить ацилированием аргинина при рН 10, а производное с защищенной гуанидиновой группой - только из диацильного производного через соответствующий N-карбоксиангидрид. Большинство л-нитрокарбобензоксиаминокислот представляет собой хорошо кристаллизующиеся соединения. [22]
Функциональные группы фермента ( карбоксильные группы, аспарагиновой и глютаминовой кислот, аминогруппы лизина, гуанидиновые группы аргинина, дисульфидные группы цистеина, неполярные белковые цепи) находятся в различных местах цепей белковой молекулы, образующей третичную и нередко четвертичные структуры, которые весьма гибки и изменяются при взаимодействии фермента с молекулами субстратов. [23]
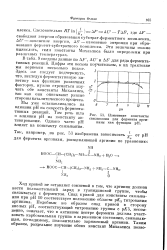 |
Изменение копстанты связывания для фермента аргиназы как функции рН. [24] |
Ход кривой не оставляет сомнений в том, что аргинин должен нести положительный заряд в гуанидиновой группе, чтобы связываться с ферментом. Спад кривой для конста-нты связывания при рН 10 соответствует положению области рК3 титрования аргинина. Подобным же образом спад кривой в сторону кислых рН, соответствующий титрованию группы с рК5, несомненно, означает, что в активном центре фермента должна участвовать карбоксильная группа в заряженном состоянии, связывающая, по-видимому, положительно заряженный аргинин. [25]
Аналогичным путем из №, № - дикарбобензоксиаргинина через N-карбоксиангидрид [2670] получают производное аргинина с защищенной гуанидиновой группой. [26]
Сакагути [342] приводит экспериментальные данные, указывающие на возможное наличие в белках связей, в которых участвует гуанидиновая группа аргинина. Подобная связь, по-видимому, должна легко гидролизоваться кислотой. [27]
Ли и сотрудники осуществили синтез гептадекапептидного и нонадекапептидного фрагментов АКТГ, используя для защиты е-аминогруппы лизина и гуанидиновой группы аргинина тозильную группу. [28]
В работе [166] показано, что защищенное по Ыа-и карбоксилу производное аргинина со свободной ( непротонированной) гуанидиновой группой дает с активированным эфиром бензилоксикарбонилглицина МШ М5 - диацильное производное, которое может дальше перацилироваться с Z-Phe-OH / ДЦГК. [29]
Эти методы также не вполне специфичны, так как окрашенные соединения получаются и с другими веществами, содержащими гуанидиновые группы, в частности, с продуктом расщепления стрептомицинов - стрептидином, не обладающим антибактериальной активностью. [30]
Страницы: 1 2 3 4