Карбонильная группа
Cтраница 1
Карбонильные группы, входящие в алифатические семичленные циклы, имеют обычные частоты колебаний, очень близкие к частотам, характерным для соединений с открытой цепью. Это было показано Шеллом и его сотрудниками при исследовании циклических кетонов в связи с изучением химии пенициллина [41], а затем подтверждено другими исследователями. [1]
Карбонильные группы в хромофорах обычно сопряжены с двойными связями или ароматическими кольцами, так что валентные колебания сдвигаются в сторону низких частот карбонильной области. [2]
Карбонильная группа в карбоксиле инертна. [3]
Карбонильная группа очень легко вступает в реакцию конденсации с аминогруппой. [4]
Карбонильная группа в кетонах значительно менее реакционно-способна, чем концевая карбонильная группа в альдегидах. Кетоны более стабильны и подвергаются реакциям присоединения менее активно, чем альдегиды. [5]
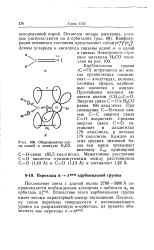 |
Общепринятая схема связей в молекуле Н2СО. [6] |
Карбонильная группа ( С О) встречается во многих органических соединениях - альдегидах, кетонах, сложных эфирах, карбоно-вых кислотах и амидах. Простейшим кетоном является ацетон ( СН3) 2С О. Энергия связи С О в Н2СО равна 166 ккал / моль. При замещении С - Н - связи связью С - С энергия связи С О возрастает. Средняя энергия связи С О составляет в альдегидах 176 ккал / моль, в кетонах 179 ккал / моль. [7]
Карбонильная группа предполагает наличие в соединении двойной связи углерод-кислород. Кислородная связь означает, что два атома углерода соединены друг с другом кислородным мостиком. Простой эфир и остальные категории трактуются в обычном понимании. [8]
Карбонильная группа поглощает в УФ-свете, и весьма вероятно, что в процессах УФ-деструкции она будет подвергаться превращениям или отщепляться от молекулы. Кроме того, возможен также распад, других связей с образованием карбонилов. В таких случаях интенсивность поглощения валентных колебаний карбонильной группы может изменяться в зависимости от природы и степени деструкции, обеспечивая высокую чувствительность при наблюдении за процессом деструкции. Частота валентных колебаний карбонильной группы также весьма чувствительна к изменениям молекулярного окружения. Даже если сами карбонильные группы и не подвергаются деструкции, они могут служить в качестве индикатора степени воздействия на молекулу. [9]
Карбонильная группа в соединениях ряда мочевой кислоты и ксантина, связанная одновременно и с углеродом и с азотом, восстанавливается до метиленовой группы совершенно аналогичным путем. [10]
Карбонильные группы атакуются электрофилами и нуклеофилами, поэтому реакции часто обратимы и ведут к последующим реакциям. Поэтому об образовании полумеркап талей нельзя говорить однозначно. [11]
Карбонильные группы могут находиться в молекуле и в других положениях. Относительное положение карбонильных групп влияет на свойства соединений. Соединения, содержащие карбонильные группы в а-положении, вследствие сопряжения я-связей окрашены в желтый цвет. [12]
Карбонильные группы могут находиться в молекуле и в других положениях. Относительное положение карбонильных групп влияет на свойства соединений. Соединения, содержащие карбонильные группы в сс-положении, вследствие сопряжения я-связей окрашены в желтый цвет. [13]
Карбонильные группы могут находиться в молекуле и в других положениях. Относительное положение карбонильных групп влияет на свойства соединений. Соединения, содержащие карбонильные группы в а-положении, вследствие сопряжения л-связей окрашены в желтый цвет. [14]
Карбонильная группа в производных карбоновых кислот вследствие сильной поляризации связи С О может подвергаться как нуклео-фильной так и электрофильной атаке. Поэтому реакции обмена имеют место как при основном, так и при кислстнсм катализе. Такой комплекс образуется в результате соединения реагирующих молекул. Последующий распад этого комплекса приводит к образованию продуктов реакции обмена. [15]
Страницы: 1 2 3 4