Дальнейшее алкилирование
Cтраница 2
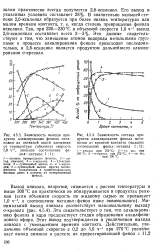
Образование этих продуктов может быть объяснено процессами изомеризации смкрезола и 2 6-ксиленола на окиси алюминия, а также их дальнейшим алкилированием избытком метанола. При низких температурах скорость изомеризации незначительна и в продуктах реакции не обнаруживается побочных продуктов. С повышением температуры скорость изомеризации возрастает, и при 350 С она становится выше скорости алкилирования фенола. [16]
Получается при взаимодействии 3 4-дихлорфенилизоцианата с 0ЛЛдиметил-гидроксиламином; или с 0-метилгидроксюгамином, А - метилгидроксиламином или незамещенным гидроксиламином при дальнейшем алкилировании первоначально образующейся мочевины. [17]
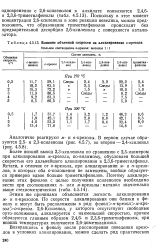 |
Влияние объемной скорости на алкилирование о-крезола Мольное соотношение о-крезол. метанол. [18] |
Более низкий выход 2 3-ксиленола по сравнению с 2 5-изомером при алкилировании ж-крезола, по-видимому, обусловлен большей скоростью его дальнейшего алкилирования в 2 3 6-триметилфенол. Кстати, в отличие от о-крезола, при алкилировании м - и / г-крезо-лов, в которых оба о-положения не замещены, вообще образуется примерно вдвое больше триметилфенолов. [19]
В процессах алкилирования бензола этилеяом и пропиленом на хлориде алюминия, кроме основных продуктов - этилбензола и изопропилбензола, образуются продукты дальнейшего алкилирования - полиалкилбензолы, основную массу которых составляют изомеры диэтил - и диизопропилбензола. [20]
Эти данные свидетельствуют о том, что замещение атомов водорода метальными группами в процессе алкилирования фенола происходит последовательно, и 2 6-ксиленол является продуктом дальнейшего алкилирования о-крезола. [22]
Синтез меркаптанов часто предпочитают проводить, исходя из тиомочевины по второй реакции вместо того, чтобы прямо получать их из NaSH, так как в последнем случае всегда имеется вероятность дальнейшего алкилирования образующегося меркаптана в тиоэфир. [23]
Образование циклических аминов из 1 4 -, 1 5 - и 1 6-дигалоген-алканов и аммиака или аминов, как правило, протекает гладко; однако в том случае, когда продуктом реакции является вторичный амин, может происходить дальнейшее алкилирование. [24]
Принципиальная технологическая схема двухстадийного сернокислотного алкилирования дикрезольной фракции представлена на рис. 4.5.2. На первой стадии при 88 С и мольном соотношении дикрезольная фракция: изобутилен 1: 1 получают в основном мо-нобутилкрезолы, которые после выделения побочных продуктов подвергают дальнейшему алкилированию на следующей стадии. Здесь примерно в тех же условиях ( температура 88 Q мольное соотношение моно-трет-бутилкрезолы: изобутилен 1: 1 3) образуются 2 6-ди-трет - бутил-ж - и - л-крезолы. Ионол, отгоняемый с верха ректификационной колонны, используют как товарный продукт, а 2 6-ди-тр. Образовавшийся ж-крезол подвергают ректификации для получения товарного продукта 99 % - ной концентрации. [25]
Этилдекаборан был получен по газофазной реакции декаборана с бромэтилом при 210 - 230 С. Дальнейшее алкилирование приводит к получению 1 2 - и 2 4-этилдекаборанов. [26]
При действии галоидных алкилов, алкилсульфатов или диазометана на аминокислоты получаются моно - или ди - М - ал-килзамещенные, называемые также вторичными и третичными аминокислотами. При дальнейшем алкилировании могут получаться четвертичные аммониевые основания. [27]
При действии галоидных алкилов, алкилсульфатов или диазометана на аминокислоты получаются моно - или ди - М - ал-килзамещенные, называемые также вторичными и третичными аминокислотами. При дальнейшем алкилировании могут получаться четвертичные аммониевые основания. [28]
При действии галоидных алкилов или алкилсульфатов на аминокислоты получаются моно - и диалкилзамещенные ( при азоте) соединения, иначе называемые вторичными и третичными аминокислотами. При дальнейшем алкилировании могут получаться четырехзамещенные аммониевые основания. [29]
Распад неустойчивых алкилов Ti ( IV) происходит быстро уже при комнатной температуре, приводя к образованию 3 - TiCl3 и смеси газообразных продуктов. Под действием триалкилалюми-ния может идти дальнейшее алкилирование и восстановление TiCls. Глубина восстановления титана зависит от природы А1 - ор-ганического соединения и соотношения Al / Ti. Триалкилы алюминия при Al / Ti 1 восстанавливают Т1С14 до Т1С12 ( рис. IV-4) и даже глубже. [30]
Страницы: 1 2 3 4