Трансаннулярная дегидроциклизация
Cтраница 1
Трансаннулярная дегидроциклизация самого циклододекана с об -, разованием диметилнафталинов происходит в незначительной степени. [1]
Трансаннулярная дегидроциклизация в ряду алкилцнкланов со средним размером кольца имеет направленный характер: преимущественное направление этого процесса определяется не наличием водородного атома при третичном атоме углерода кольца, а связано, по-видимому, с конформационны-ми особенностями цикланов. Действительно, при дегидроциклизации ме-тплциклооктана преобладает образование 1-метилпенталана, в то время как из метилциклононана в тех же условиях преимущественно образуется би-циклический углеводород с ангулярным положением метильной группы, а дегидроциклизация метилциклодекана приводит, по-видимому, в основном к 9-и 1-метилдекагидроазуленам. Если допустить, что указанные возможности образования метилпенталанов равновероятны, то катализат метилциклооктана должен был содержать 1-метилпенталана вдвое больше, чем 2-метил - или 7-метилпенталана. Действительно, в этом случае в катали-зате преобладает 1-метилпенталан. [2]
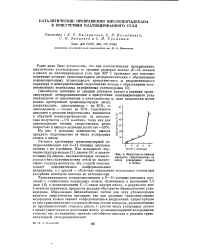 |
Зависимость выхода. [3] |
Трансаннулярная дегидроциклизация в 8 - 11-члешшх цикланах протекает с отщеплением водородных атомов, сближенных в положении 1 5 ( или 1 6) и возникновением С-С - связи внутри цикла, в результате чего в качестве первичных продуктов реакции образуются бициклические углеводороды. Образование бициклических систем для этих углеводородов является энергетически выгодным, так как удаление трансаннулярных водородных атомов снимает конформационное напряжение, существующее за счеттрансаннулярного взаимодействия атомов водорода, расположенных на противоположных сторонах цикла. С ростом числа углеродных атомов в цикле увеличивается расстояние между трансаннулярными водородными атомами, что, по-видимому, снттжает способность циклана к реакции трансаннулярной дегидроциклизации. [4]
Реакции трансаннулярной дегидроциклизации проводят в жестких условиях. При этом первичные продукты этих реакций подвергаются дальнейшим превращениям, образуя производные бензола или нафталина. [5]
Реакции трансаннулярной дегидроциклизации и гидрогенолиза цикла являются, очевидно, конкурирующими: для 8 - 11-членных цикланов, в силу их конформационных особенностей, с большой легкостью протекает трансаннулярная дегидроциклизация, и ее скорость превышает скорость гидрогенолиза. В случае 12-членного циклана, не имеющего столь благоприятного строения для реакции трансаннулярной дегидроциклизации, скорости этих двух конкурирующих реакций становятся примерно одинаковыми. Большие циклы вообще лишены трансаннулярного взаимодействия противолежащих водородных атомов, и в случае справедливости приведенных соображений для них должна быть затруднена трансаннулярная дегидроциклизация, а реакция гидрогенолиза может явиться основным направлением превращений. [6]
Реакции трансаннулярной дегидроциклизации проводят в жестких условиях. При этом первичные продукты этих реакций подвергаются дальнейшим превращениям, образуя производные бензола или нафталина. [7]
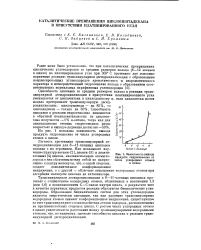 |
Зависимость выхода. [8] |
Легкость протекания трансаннулярной дегидроциклизации для 8 - 11-членных цикланов связана с их строением. [9]
Таким образом, трансаннулярная дегидроциклизация в ряду метил-цикланов со средним размером кольца имеет направленный характер: преимущественное направление этого процесса определяется не наличием водородного атома при третичном атоме углерода кольца, а связано, по-видимому, с конформационными особенностями цикланов. Действительно, при дегидроциклизации метилциклооктана преобладает образование 1-метилпенталана, в то время как для метилциклононана в тех же условиях преимущественно образуется бициклический углеводород с ангулярным положением метильной группы, а дегидроциклизация метилциклодекана приводит, вероятно, в основном к 9-метил - и 2-метил-декагидроазуленам. [10]
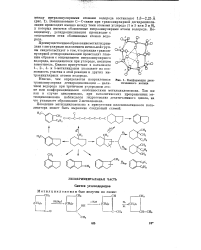 |
Конформация девя-тичлевного кольца. [11] |
Неясно, чем определяется направленная трансаннулярная дегидроциклизация - наличием водорода при третичном углеродном атоме или конформационными особенностями метилциклононана. Так же как в случае циклононана, при каталитических превращениях метилциклононана наблюдался гидрогенолиз девятичленного цикла, на что указывает образование 2-метилнонана. [12]
При рассмотрении способности 8 - 12-членных циклов к трансаннулярной дегидроциклизации следует, вероятно, учитывать и тот факт, что образование бициклического углеводорода снимает напряжение, возникающее вследствие отталкивания противолежащих атомов водорода и, следовательно, является энергетически выгодным для 8 - 12-членных циклов. [14]
Основной первичной реакцией метилциклодекана в присутствии платинированного угля является трансаннулярная дегидроциклизация, ко-торая протекает в двух направлениях: 1) осуществляется Cs-дегидро-диклизация с образованием метилдекагидроазуленов, 2) происходит CG-дегидроциклизация, которая приводит к метилдекалинам и метилнаф-талинам. Так же, как в случае циклодекана, для метилциклодекана в большей степени характерна С5 -, нежели С6 - дегидроциклизация, так как вещества, образовавшиеся в результате первой реакции, составляют в сумме свыше 70 % от веса продуктов превращений, Метилдекагидроазу-лены в условиях опыта неустойчивы и претерпевают дальнейшие превращения. По-видимому, за счет вторичных превращений метилдекагидроазуленов образуется о-метилизопропилбензол, составляющий по весу почти половину продуктов превращений метилциклодекана. Вследствие вторичных превращений этих же углеводородов можно объяснить и присутствие в катализате метилдиэтилбензолов и 5-метилиндана. [15]
Страницы: 1 2 3 4
