Трансаннулярная дегидроциклизация
Cтраница 4
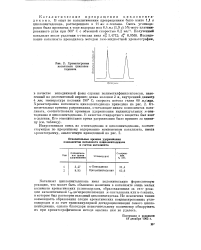 |
Хроматограмма катализата циклопен-тадекана. [46] |
Катализат циклопентадекана имел положительную формолитовую реакцию, что может быть объяснено наличием в катализате очень малых количеств ароматических углеводородов, образовавшихся за счэт реакции каталитической Св-дегидроциклизации к-пентадекана или к-гексана, в котором был растворен исходный циклопентадекан. Не исключена также возможность образования следов ароматических конденсированных углеводородов и за счет трансаннулярной дегидроциклизации самого циклопентадекана, однако благодаря незначительному количеству обнаружить их при хроматографическом методе анализа нам не удалось. [47]
При пропускании циклооктана над алюмохромовым катализатором при 420 С в токе водорода образуются г / ис-пенталан, этилбензол, о -, м - и re - ксилолы. Образование каждого из этих углеводородов, по мнению авторов, связано с трансаннулярной дегидроциклизацией циклооктана. [48]
Бицикло - ( 0 4 6) - додекан далее дегидрируется в бензциклооктан. На основании работы Казанского, Шоковой, Хромова, Алексаняна и Стерина [3] по каталитическим превращениям циклооктана над платинированным углем можно предположить, что бензциклооктан далее претерпевает трансаннулярную дегидроциклизацию в 1 2-бензбицикло - ( 0 3 3) - октан. [49]
Как показало исследование структуры циклододекана ( рис. 3), в нем уже нет заметного трансаннулярного взаимодействия противолежащих атомов водорода, а наикратчайшее расстояние между атомами водорода составляет 2 1 А. Если полагать, что трансаннулярная дегидроциклизация протекает с отщеплением сближенных атомов водорода, то рост размера кольца и увеличение расстояния между трансаннулярными водородными атомами должны снижать способность циклана к реакции трансаннулярной дегидроциклизации. [50]
В литературе отсутствуют данные о конформационных особенностях одиннадцатичленного кольца. Это обстоятельство свидетельствует о том, что в циклоундекане имеются, по-видимому, сближенныетрансаннулярные атомы водорода и поэтому для него, так же как для рассмотренных выше цикла-нов, должна легко протекать трансаннулярная дегидроциклизация. Цик-лоундекан при контакте с платинированным углем при 300 С претерпевал на 15 % непосредственный гидрогенолиз кольца с образованием - ундекана и дегидроциклизацию в траяе-бицикло ( 5 4 0) ундекан, который в условиях опыта далее превращался в бензсуберан. [51]
Продукты превращений циклоундекана при 200 С состояли изцик-лодекана, циклононана, н-ундекана, - декана и бицикло ( 5 4 0) ундекана. Бицикло ( 5 4 0) ундекан явился продуктом трансаннулярной дегидроциклизации исходного циклоундекана. [52]
Реакции трансаннулярной дегидроциклизации и гидрогенолиза цикла являются, очевидно, конкурирующими: для 8 - 11-членных цикланов, в силу их конформационных особенностей, с большой легкостью протекает трансаннулярная дегидроциклизация, и ее скорость превышает скорость гидрогенолиза. В случае 12-членного циклана, не имеющего столь благоприятного строения для реакции трансаннулярной дегидроциклизации, скорости этих двух конкурирующих реакций становятся примерно одинаковыми. Большие циклы вообще лишены трансаннулярного взаимодействия противолежащих водородных атомов, и в случае справедливости приведенных соображений для них должна быть затруднена трансаннулярная дегидроциклизация, а реакция гидрогенолиза может явиться основным направлением превращений. [53]
Трансаннулярная дегидроциклизация в 8 - 11-члешшх цикланах протекает с отщеплением водородных атомов, сближенных в положении 1 5 ( или 1 6) и возникновением С-С - связи внутри цикла, в результате чего в качестве первичных продуктов реакции образуются бициклические углеводороды. Образование бициклических систем для этих углеводородов является энергетически выгодным, так как удаление трансаннулярных водородных атомов снимает конформационное напряжение, существующее за счеттрансаннулярного взаимодействия атомов водорода, расположенных на противоположных сторонах цикла. С ростом числа углеродных атомов в цикле увеличивается расстояние между трансаннулярными водородными атомами, что, по-видимому, снттжает способность циклана к реакции трансаннулярной дегидроциклизации. [54]
Превращения углеводородов со средним размером кольца в присутствии платинового катализатора протекают в двух независимых направлениях: трансаннулярной дегидроциклизации и прямого гидрогенолиза кольца. На первой стадии трансаннулярной дегидроциклизации образуется бици-клический углеводород, природа которого в основном определяется кон фор-мационными особенностями исходного циклана. Бициклические углеводороды в условиях опыта претерпевают дальнейшие превращения: ароматизацию, гидрогенолиз пяти - и изомеризацию семичлениых циклов, в результате чего наблюдается весьма сложный состав реакционной смеси. Для метилцикла-нов с 8 - 10-членными кольцами трансаннулярная дегидроциклизация имеет направленный характер: преимущественное направление каталитического процесса определяется конформацией исходного углеводорода. [55]
В циклононане ( см.рис. 1) заместители, вероятно, могут занимать лишь экстрааннулярные положения. Как показывают данные рентгеноструктур-ного анализа, среди экстрааннулярных положений заместителя имеются наиболее предпочтительные. Таким, например, является положение заместителя при Q. С предпочтительным положением метильной группы в де-вятичленном кольце связано, по-видимому, и преимущественное образование 8-метилгидриндана при трансаннулярной дегидроциклизации метилциклононана. [56]
Метилгидриндан мог образоваться за счет трансаннулярной дегидрогенизации исходного метилциклононана с участием водорода при третичном атоме углерода, несущем метальный заместитель. Отщепление метильной группы в 8-метилгидриндане при катализе ведет к образованию гидриндана, а дегидрогенизация шестичленного кольца в последнем - к индану. Гидрогенолиз дятичленного цикла в 8-метилгидриндане приводит к получению диметилэтилциклогексанов. Таким образом, - 50 % от веса катализата составляют tyuc - 8-метилгидриндан и вторичные продукты его превращений, а отсюда следует, что для метилциклононана характерен такой тип трансаннулярной дегидроциклизации, при котором происходит преимущественное образование метилгидриндана с ангулярным положением метильной группы. [57]
Страницы: 1 2 3 4