Действие - заместитель
Cтраница 1
Действие заместителей, связанных с карбонильной группой, можно также рассматривать как происходящую внутри функциональной группы компенсацию влияния карбоннла; при этом электронооттягивающее влияние карбонильного кислорода ( - М, - /) проявляется все в меньшей степени при переходе от кислород-аниона к алкоксигруппе. Водород в альдегидной группе практически не действует, в то время как хлор в хлор-ангидридах даже препятствует электростатически этому электронному сдвигу. [1]
Действие заместителя на фталил прямое и идет по сопряженной системе в отличие от заместителей в фенильном кольце, что приводит к потере гемолитической составляющей на фталиле, определяющей физиологическую активность. Не исключена возможность, что сочленение донора с ароматическим кольцом акцептора даст физиологически активные соединения, но необходимым условием по-прежнему будет их акопланарность. [2]
Подобного рода действие заместителя впервые обнаружено в реакциях эпоксидирования непредельных спиртов надкислота-ми. Согласно Хенбесту и Вильсону [276], при взаимодействии указанных реагентов образуется переходный комплекс, стабилизированный водородной связью, возникающей между гидроксиль-ной группой непредельного спирта и одним из атомов кислорода надкислоты. Следствием соучастия гидроксильной группы является ускорение реакции эпоксидирования с получением окиси, ориентация эпоксигруппы в которой совпадает с ориентацией гидроксила. [3]
Активирующее и орто геара-ориентирующее действие алкилышх заместителей также может быть понято на основе представления об индуктивных эффектах ( см., однако, стр. Так, промежуточные соединения при орто -, пара - и лшгаа-замещении толуола должны быть стабилизированы вследствие того, что метильная группа способна подавать электроны ( / - эффект) и частично компенсировать таким образом положительный заряд. [4]
Приняв во внимание индукционное и мезомерное действие заместителей и воспользовавшись простым методом ЛКАО МО, он рассчитал электронные плотности q в м - и - положениях серии моноза-мещенных бензола, действительно обнаружив пропорциональность между qM и ам, qa и ап. [5]
Значительно смещается под действием заместителей, что не может быть строго объяснено vC - С. [6]
Ряд средней активности показывает действие заместителей на легкость, с которой этиленовое производное реагирует со средним радикалом, и на стабилизацию образующегося радикала. [7]
Во всех этих случаях особое действие заместителя устанавливают прежде всего благодаря тому, что для каждого изучаемого случая выясняют, является ли отклонение от нормального действия заместителя ( относительно наблюдаемого обычно) значительным или нет. В качестве подобного стандарта могут служить, например, зависимости Гаммета или Тафта. [8]
Как правило, под действием внешнесферного заместителя происходит несильное изменение в положении полос поглощения в ИК-спектре. Однако, если внешнесферный ион имеет тенденцию к Н - связеобразованию с аддендом, то такого рода взаимодействие неминуемо скажется на характере колебаний внутрисферной группы, что в свою очередь ведет к смещению полосы поглощения. Так, в ряду СЮ - NO f, I -, Вг -, С1 - слева направо увеличивается тенденция к образованию водородных связей. [9]
Активирующее ( или дезактивирующее) действие заместителя X в соединении С6Н5Х распространяется неравномерно на пять незамещенных атомов бензольного кольца, вследствие чего вступление нового заместителя в орто -, мета - или гаара-положение к уже имеющемуся будет происходить с разной скоростью в зависимости от свойств группы, стоящей в ядре. Поскольку переходное состояние обычно имеет много общего в энергетическом отношении с соответствующим метастабильным промежуточным продуктом или а-комплексом, можно считать, что они сходны также ив структурном отношении. Исходя из этого можно ожидать, что структурные особенности, способствующие стабилизации определенного а-комплекса, должны стабилизировать также и соответствующее переходное состояние. [10]
Активирующее ( или дезактивирующее) действие заместителя X в соединении СвН5Х распространяется неравномерно на пять незамещенных атомов бензольного кольца, вследствие чего вступление нового заместителя в орто -, мета - или пара-положение к уже имеющемуся будет происходить с разной скоростью в зависимости от свойств группы, стоящей в ядре. Поскольку переход ное состояние обычно имеет много общего в энергетическом отношении с соответствующим метастабильным промежуточные продуктом или а-комплексом, можно считать, что они сходны также ив структурном отношении. Исходя из этого можно ожидать, что структурные особенности, способствующие стабилизации определенного а-комплекса, должны стабилизировать также и соответствующее переходное состояние. [11]
DGEBA), то под действием заместителей отдельные звенья цепи должны будут отодвигаться друг от друга, что вызовет изменение количества первоначально присутствующих атомов в местах поперечных сшивок и приведет к уменьшению количества поперечных связей в единице объема полимера. [12]
При этом было показано, что действие заместителей в бензольном кольце на боковую цепь, в данном случае на атом фтора, передается через изменение заряда 6 узлового атома углерода, к которому присоединен атом фтора. [13]
На примере галогенов отчетливо видно возрастание действия заместителя с ростом его электроотрицательности в случае, когда только один атом углерода отделяет его от изопропильной группы. Эффект резко уменьшается, если между заместителем и рассматриваемой связью появляется еще один атом углерода. Существует прямая связь этих данных с имеющимися в литературе другими величинами, характеризующими электроотрицательность галогенных заместителей. [14]
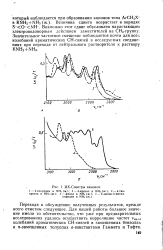 |
ИК-Спектры анионов. [15] |
Страницы: 1 2 3 4