Аллил-катион
Cтраница 2
 |
Схема иллюстрирует связь между высокой реакционной способностью аллил-хлорида в реакциях SN. по сравнению с к-пропилхлоридом и низкой энергией образования аллил-катиона. [16] |
Таким образом, энергия аллил-катиона ниже, чем, энергия и-пропил-катиона; из рис. 11 - 7 очевидно, что для образования аллил-катиона из аллилхлорида требуется меньше энергии, чем для образования к-пропил-катиона из к-про-пилхлорида. При этом важно иметь в виду, что легкость протекания реакции определяется различием энергий карбокатиона и исходного галогенида, но не различием энергий карбокатионов друг относительно друга. [17]
Эти продукты образуются из симметричного аллил-катиона, в котором обе мети-леновые группы неразличимы. [18]
Ни одпо из соединений не приводит к аллил-катиону. [19]
Геометрия, а также орбитальные модели аллена и аллил-катиона изображены ниже; очевидно, что, пока вокруг связи С - С происходит вращение, прото нйрование центрального углерода аллена не даст аллил-катиона. [20]
 |
Очертания МО аллильного радикала. [21] |
Подобная модель применима для рассмотрения других простых сопряженных частиц аллильного типа - аллил-катиона и аллил-аниона. [22]
Бензилгалогениды С6Н5СН2 - X образуют карбокатионы с сильной делокализацией заряда, вследствие чего эти катионы значительно устойчивее простых аллил-катионов. [23]
Аллилхлорид в противоположность аллил-катиону не стабилизируется вследствие резонанса, однако общая энергия аллилхлорида меньше суммы энергий отдельно взятых аллил-катиона и аниона хлора. [24]
 |
Схемы спаривания электронов в аллил-катионе. [25] |
Трудности, связанные с качественным применением теории молекулярных орбиталей к простым системам, можно видеть также на хорошо известном примере аллил-катиона, который был рассмотрен ранее с помощью метода резонанса ( стр. Качественная картина молекулярных орбиталей предполагает, что два электрона распределены более или менее равномерно по трем орбиталям, причем, очевидно, на каждом углеродном атоме должен находиться частичный положительный заряд. Это не соответствует экспериментальным фактам ( а также более подробному расчету по методу ЛКАО), из которых следует, что заряд расположен главным образом, если не целиком, на концевых атомах углерода. [26]
 |
Атомно-орбитальная модель л-электронной системы ал-кил-катиона.| Схемы спаривания электронов в аллил-катионе. [27] |
Трудности, связанные с качественным применением теории молекулярных орбиталей к простым системам, можно видеть также на хорошо известном примере аллил-катиона, который был рассмотрен в разд. Качественная картина молекулярных орбиталей предполагает, что два электрона распределены более или менее равномерно по трем орбиталям, причем, очевидно, на каждом углеродном атоме должен находиться частичный положительный заряд. Это не соответствует экспериментальным фактам ( а также более подробному расчету по методу ЛКАО), из которых следует, что заряд расположен главным образом, если не целиком, на концевых атомах углерода. [28]
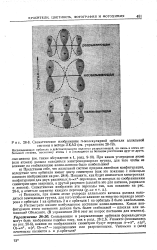 |
Схематическое изображение я-молекулярной орбитали алдильной. [29] |
При каком углеродном атоме ( или атомах) должна находиться электронодонорная группа, для того чтобы ее влияние на стабилизацию аллил-катиона было наибольшим. [30]
Страницы: 1 2 3 4