Дихлорбутен
Cтраница 2
Смесь дихлорбутенов перегоняют в колонне 22, отбирая 90 % от указанного потенциального содержания. [16]
Определению не мешают дихлорбутены, моновинилацетилен, хлорбензол, ацетилен, этилцеллозольв, оксид и диоксид углерода, диоксид серы, оксиды азота. [17]
В данной работе содержащий дихлорбутен комплекс хлорида меди ( I) получен путем обменного взаимодействия в жидкой фазе между 1 4-дихлорбутеном - 2 и растворимым комплексом хлорида меди ( I) с акрилонитрилом при комнатной температуре в отсутствии кислорода. Комплекс представляет бледно-зеленое кристаллическое вещество, нерастворимое в избытке олефина, углеводородах и хлоралканах. Взаимодействие комплекса с сильными донорами, например с третичными аминами, а также его термическое разложение при температурах 50 - 80 С приводит к образованию сме си изомерных дихлорбутенов, близкой к равновесной. Разложение комплекса под действием диэтиламина происходит с выделением тепла и на воздухе сопровождается мгновенным окислением меди до двухвалентной. [18]
При быстром добавлении дихлорбутена энергичное выделение тепла может привести к выбросу реакционной массы и даже к взрыву. [19]
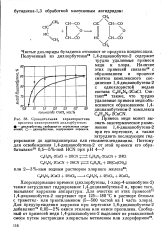
II) из дихлорбутена ( I) в качестве омыляющего агента нами были исследованы водные растворы гидроокисей щелочных и щелочноземельных металлов, соли слабых кислот и сильных оснований, а также вода. Омыление дихлорбутена ( I) даже 1 % раствором гидроокиси натрия приводит к образованию твердого полимера. Однако, если раствор гидроокиси натрия вводить постепенно и, что особенно важно, поддерживая в системе значение рН постоянным и равным 7, можно получить изомерные бутендиолы с выходом 40 % при полной конверсии исходного дихлорбутена. [20]
После прибавления всего дихлорбутена нагревание продолжают еще 1 час. [21]
При быстром добавлении дихлорбутена энергичное выделение тепла может привести к выбросу реакционной массы и даже к взрыву. [22]
 |
Сравнительная характеристика. [23] |
Хлор содержащие примеси ( дихлорбутены, 1-хлор - 4-цианобутен - 2) также затрудняют гидрирование 1 4-дицианобутена - 2 и, кроме того, вызывают коррозию аппаратуры. [24]
С повышением температуры выход дихлорбутенов снижается ( за счет образования тетрахлорбутена); при низких температурах преобладает 1 2-изомер. В присутствии катализаторов кислотного типа ( ZnCl2 и др.) эти изомеры способны переходить друг в друга с образованием равновесной смеси, содержащей 70 % 1 4-изомера. [25]
Из рассмотренных методов получения дихлорбутенов наибольший интерес представляют газофазное хлорирование и хлорирование переносчиками хлора. Выход дихлорбутенов в обоих методах превышает 90 %, однако продукт-сырец, полученный при хлорировании переносчиками хлора, содержит - 98 % основного вещества и может быть использован в синтезе 1 4-дицианобутена - 2 без дополнительной очистки. Это делает процесс хлорирования бутадиена переносчиками хлора наиболее перспективным для получения дихлорбутенов. [26]
С повышением температуры выход дихлорбутенов снижается за счет образования тетрахлорбутена; при низких температурах преобладает 1 2-изо-мер. В присутствии катализаторов кислотного типа ( BF3, ZnCb и др.) эти изомеры способны переходить друг в друга с образованием равновесной смеси, содержащей 70 % 1 4-изомера. [27]
Основные технологические параметры процесса получения дихлорбутенов хлорированием бутадиена в расплаве СиС12 - CuCl - КС1 следующие: температура 325 - 330 С, время контакта 10 - 15 с. При использовании для хлорирования расплава, содержащего 45 % СиС12, 35 % CuCl и 20 % КС1, в продукте - сырце содержится более 98 % дихлорбутенов. [28]
Выход основного побочного продукта - дихлорбутена - оставляет 3 - 4 % от выхода прореагировавшего винилацетилена. [29]
При хлорировании бутадиена получается смесь обоих изомерных дихлорбутенов, в которой при низких температурах преобладает 1 2-изомер. Таким образом, осуществляя дополнительную изомеризацию одного из дихлорпроизводных, можно получать другой в качестве единственного целевого продукта. [30]
Страницы: 1 2 3 4