Исследование - кинетика - электродный процесс
Cтраница 4
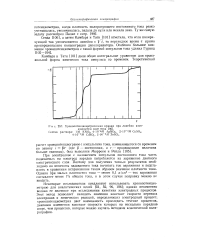 |
Хронопотенциометрическая кривая при линейно изменяющейся силе тока. [46] |
Некоторые исследователи предлагают использовать хронопотенцио-метрию для аналитических целей [51, 52, 96, 106]; однако несомненно велико ее значение при исследовании кинетики электродных процессов. Этот метод позволяет находить значения констант скорости переноса электронов и химических реакций, определяющих электродный процесс; хронопотенциометрия дает возможность проследить течение процессов, диапазон изменения констант скорости которых на несколько порядков шире, чем процессов, которые можно изучать методами классической полярографии. [47]
Возможности применения этих методов для определения обратимости или необратимости рассматриваемого электродного процесса или, вернее, для исследования кинетики электродных процессов различны и зависят от того, в какой степени можно изменить скорость переноса вещества к электроду, применяя данный метод. [48]
 |
Схема установки длч снятия стационарных поляризационных кривых. [49] |
Так как даже незначительные количества поверхностно-активных веществ ( особенно органических) могут существенно изменять скорость электродных реакций, исследования кинетики электродных процессов следует проводить с максимально чистыми растворителями и реактивами. Их очищают обычными химическими методами, а также адсорбируя примеси на поверхности твердых тел с сильно развитой поверхностью ( платинированная платина, активированный уголь) и длительным электролизом исследуемого раствора. [50]
Вращающийся дисковый электрод с кольцом, впервые предложенный Фрумкиным и Некрасовым [1], в настоящее время находит все более широкое применение в исследовании кинетики электродных процессов, протекающих с образованием продуктов реакции в растворе. [51]
Если собственно электродный процесс протекает быстро по - сравнению, например, с процессом диффузии, TOI для изучения его закономерностей необходимо использовать специальные методы исследования кинетики электродных процессов. Методы, используемые при изучении кинетики электродных процессов, рассмотрены в следующей главе. [52]
В заключение следует еще раз подчеркнуть, что, хотя некоторые авторы рекомендуют хронопотенциометрию как аналитический метод, самое большое значение, она, по-видимому, должна иметь при исследовании кинетики электродных процессов. В этом отношении она имеет такие же возможности, как и описанные в гл. [53]
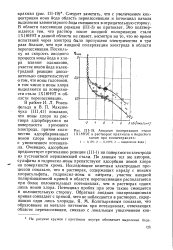 |
Анодная поляризация стали 1Х18Н9Т в растворах крахмала и йодистого. [54] |
По данным тех же авторов, сульфаты и гидроксил-ионы препятствуют адсорбции ионов хлора на поверхности хрома. Исследование кинетики электродных процессов показало, что в растворах, содержащих наряду с ионами хлорасульфаты, гидроксил-ионы и нитраты, участок анодной поляризационной кривой в области перепассивации располагается при более положительных потенциалах, чем в растворах одних лишь ионов хлора. Потенциал пробоя при этом также смещается в положительную сторону. Обратная анодная поляризационная кривая совпадает с прямой, чего не наблюдается в растворах, содержащих одни лишь хлориды. [55]
Первый пример использования измерений в нестационарных условиях для количественного исследования кинетики электродных процессов был дан в работе П. И. Долина и Б. В. Эршлера [1], определивших кинетику разряда ионов водорода ва платине по проводимости электрода по отношению к переменному току. Другими многообещающими методами исследования кинетики электродных процессов являются: метод, основанный на определении временной зависимости потенциала электрода при пропускании тока постоянной силы, впервые примененный В. А. Ройтером, В. А. Юза и Е. С. Полуяном [7], и метод определения временной зависимости тока при наложении определенной поляризации. В настоящее время вряд ли можно дать законченную сравнительную оценку эффективности перечисленных методов; несомненно, что тот или другой метод имеет преимущества при решении определенных задач. Так, переменноточные измерения особенно удобны для открытия обратимых стадий процесса, измерения с наложением тока постоянной плотности - для обнаружения медленных химических реакций, предшествующих собственно электрохимической стадии. Математическая трактовка этих методов, основанная на решении дифференциальных уравнений диффузии при краевых условиях, определяемых закономерностями протекания самого электрохимического процесса, оказывается часто весьма сложной, особенно в случае применения капельного электрода. Тот факт, что результаты этих расчетов для ряда электрохимических процессов удалось полностью подтвердить на опыте, является особенно убедительным доказательством правильности основных феноменологических предпосылок электрохимической кинетики. [56]
 |
Изменение во времени электродных потенциалов в 0 01 % - ном водном растворе бензосульфокислоты. [57] |
Конечными продуктами окисления углеводородов топлив и сернистых соединений, растворимыми в воде, являются в основном карбоновые и сульфоновые кислоты [ 299, 300, ЗОЦ. На рис. 6.6 приведены результаты исследований кинетики электродных процессов в водных растворах бензолсульфокислоты. Последняя существенно влияет на развитие катодного процесса коррозии бронзы ВБ-23НЦ, причем предельный диффузионный ток с увеличением концентрации сульфокислоты возрастает, что можно объяснить деполяризующим действием кислоты. [58]
Страницы: 1 2 3 4