Исследование - белок
Cтраница 2
 |
Электронная микрофотография препарата миозина. Увеличение в 28 000 раз. На микрофотографии хорошо видны агрегаты тончайших миозиновых нитей. [16] |
При электр о форетическом исследовании сарко-ялазматических белков в них можно обнаружить наряду с белками миоге-новой группы, в которую попадают и водонерастворимые глобулины, особую быстро двигающуюся фракцию - миоальбумин. [17]
Еще на ранней стадии исследования белков было обнаружено, что при некоторых видах их химической модификации, не приводящих к изменениям молекулярного веса, происходит значительное увеличение вязкости растворов белков. Это явление объясняется тем, что гюлипептидная цепь немодифицированного белка заспирализована и свернута, в результате чего она принимает глобулярную форму. Пример способа сворачивания приведен на рис. 40.5, на котором схематически представлена третичная структура мпоглобина, имеющего протяженные спиральные участки, чередующиеся е неспиральной, нерегулярной вторичной структурой; именно на этих участках происходит сворачивание и изгибание. Как было предсказано, а затем подтверждено рентгеноструктурным анализом, пролин вследствие своей циклической структуры образует пептидные связи с углами, исключающими спиральную структуру. [18]
Еще на ранней стадии исследования белков было обнаружено, что при некоторых видах их химической модификации, не приводящих к изменениям молекулярного веса, происходит значительное увеличение вязкости растворов белков. Это явление объясняется тем, что полипептидная цепь немодифицированного белка заспирализована и свернута, в результате чего она принимает глобулярную форму. Пример способа сворачивания приведен на рис. 40.5, на котором схематически представлена третичная структура миоглобина, имеющего протяженные спиральные участки, чередующиеся с неспиральной, нерегулярной вторичной структурой; именно на этих участках происходит сворачивание и изгибание. Как было предсказано, а затем подтверждено рентгеноструктурным анализом, пролин вследствие своей циклической структуры образует пептидные связи с углами, исключающими спиральную структуру. [19]
Естественно, что к исследованию белков - самых важных биологических полимеров - сейчас привлекается весь арсенал разнообразных физических методов, в том числе и оптических. Оптика белков - новая область молекулярной физики, развивающаяся очень быстро. Но рассеяние рентгеновых лучей остается пока что наиболее прямым методом изучения белков, хотя применять его нелегко. Впрочем, это тоже ведь оптика: рентгеновы лучи отличаются от световых лишь тем, что их длина воля много меньше, в тысячи раз меньше. [20]
Естественно, что к исследованию белков - самых важных биологических полимеров - сейчас привлекается весь арсенал разнообразных физических методов, в том числе и оптических. Оптика белков - новая область молекулярной физики, развивающаяся очень быстро. Но рассеяние рентгеновых лучей остается пока что наиболее прямым методом изучения белков, хотя применять его нелегко. Впрочем, это тоже ведь оптика: рентгеновы лучи отличаются от световых лишь тем, что их длина волн много меньше, в тысячи раз меньше. [21]
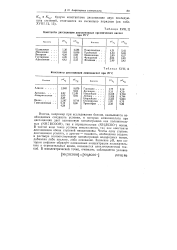 |
Константы диссоциации аминокислот при 25 С. [22] |
Иногда, например при исследовании белков, оказывается необходимым создавать условия, в которых аминокислота при диссоциации дает одинаковую концентрацию как положительных ( NHa RCOOH), так и отрицательных ( NH2RCOO) ионов. В чистой воде такое условие невыполнимо, так как константы диссоциации обеих ступеней неодинаковы. Чтобы одну ступень диссоциации усилить, а другую - подавить, необходимо создать в растворе соответствующую концентрацию водородных ионов, добавляя либо кислоту, либо основание. Значение рН, при котором амфолит образует одинаковые концентрации положительных и отрицательных ионов, называется изоэлектрической точкой. [23]
Все проведенные до настоящего времени исследования белков указывают, что молекула белка построена из а-аминокислот. Если это так, то возникает вопрос, каким образом, при посредстве каких связей соединены аминокислоты в молекуле белка. [24]
Ультрацентрифуга оказалась особенно ценной при исследовании белков, однако в то время этих приборов было очень мало. Для определения молекулярных весов было также предложено измерение осмотического давления, однако измерения по этому методу занимают много времени. [25]
Аналитическая ультрацентрифуга широко используется при исследовании вновь выделенных белков и других макромолекул. Она служит также для проверки качества препаратов, полученных установившимися методами. [26]
Другой областью применения тонкослойной гель-хроматографии является исследование белков сыворотки и других биологических жидкостей, откуда эти белки удается выделить лишь в очень небольших количествах. Вслед за элек-трофоретическим разделением в одном направлении проводят хроматографию в перпендикулярном направлении. [27]
Хорошим примером изучения нативных белков является исследование белков сыворотки крови, включающее их выделение, очистку, количественный и качественный анализ. Широкое применение методов анализа белков будет показано нами именно на примере изучения сывороточных белков. [28]
 |
Вид ( сбэку U-образной трубки в приборе Тизелиуса. а - рабочее положение. б - положение в момент заполнения верхней части.| Схема прибора Тизелиуса в собранном виде. [29] |
Метод Тизелиуса особенно широко применяется при исследовании белков и других высокомолекулярных электролитов, поскольку с его помощью можно не только определить скорость электрофореза, но и разделить смесь высокомолекулярных веществ на отдельные компоненты. В самом деле, если исследуемый раствор содержит несколько компонентов с различными электрофоретическими полвижностями, то фронт передвижения более подвижных компонентов будет обгонять фронт движения компонентов, движущихся медленнее, и образуется столько границ, сколько компонентов в смеси. [30]
Страницы: 1 2 3 4