Карбид - кобальт
Cтраница 2
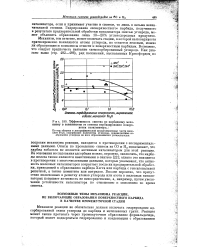 |
Эффективность синтеза по карбидному механизму в зависимости от степени карбидирования поверхности катализатора. 1. [16] |
Опыты по проведению синтеза из СО и Н2 показывают, что карбид кобальта не является активным катализатором для этой реакции. На основании исследования адсорбции можно, вероятно, заключить, что карбиды железа также являются неактивными в синтезе [22]; однако это находится в противоречии с многочисленными данными, которые указывают, что активность железных катализаторов возрастает после их предварительной обработки, приводящей к образованию карбида Хэгга или карбида с гексагональной решеткой, а также цементита или нитридов. Вполне вероятно, что присутствие включенных в решетку атомов углерода или азота в железных катализаторах повышает активность не непосредственно, а, например, путем увеличения устойчивости катализатора по отношению к окислению во время синтеза. [17]
Позднее, в 1947 г., Крэксфорд высказал иное предположение об образовании карбидов кобальта как промежуточных продуктов при синтезе, полагая, что вначале происходит - хемосорбция окиси углерода на поверхности металла с присоединением углеродного атома непосредственно к металлу. Кислородный атом хемосорбированной молекулы удаляется в виде воды. [18]
Позднее, в 1947 г., Крэксфорд высказал иное предположение об образовании карбидов кобальта как промежуточных продуктов при синтезе. Он полагает, что вначале происходит хемосорбция окиси углерода на поверхности металла с присоединением углеродного атома непосредственно к металлу. [19]
Все соли кооалыосинеродистоводороднои кислоты разлагаются при прокаливани-и, после чего остаются цианид и карбид кобальта. Щелочные и щелочноземельные соли окрашивают перл буры в окислительном и восстановительном пламени в синий цвет. [20]
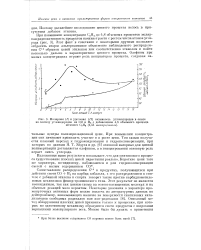 |
Молярная ( / и удельная ( / / активность углеводородов в опыте. [21] |
Сопоставление распределения С14 в продуктах, получающихся при действии смеси СО Н2 на карбид кобальта, с его распределением в синтезе с добавкой этилена и спирта говорит также против карбиднометиле-новых механизмов фишер-тропшевского типа. Этот результат не является неожиданным, так как ценные схемы па основе насыщенных молекул и их обычных реакций мало вероятны. Описанный метод обнаружения плоских цепей применим только к процессам, при которых но однотипному механизму образуются смеси продуктов с широкими вариациями молекулярного веса. [22]
Следовательно, при синтезе жидких углеводородов из окиси углерода и водорода над кобальтовыми и никелевыми катализаторами карбиды кобальта и никеля не являются ни промежуточными продуктами, ни катализаторами реакции синтеза. [23]
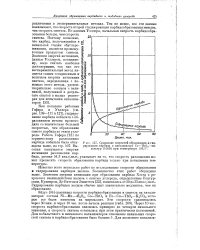 |
Сравнение скоростей образования и гидрирования карбида в катализаторе Со-ThOa - кизельгур ( 108В при температуре 199 5. [24] |
Как показано работами Гофера и Уэллера ( см. рис. 109 - 111 и 127), гидрирование карбида кобальта с образованием метана происходило со значительно большей скоростью, чем образование самого карбида из окиси углерода. Работа Гофера [12] по термическому разложению карбида кобальта была обсуждена выше, на стр. Высокая кажущаяся энергия активации разложения карбида, равная 54 3 ккал / молъ, указывает на то, что скорость разложения может превысить скорость образования карбида только при повышении температуры. [25]
При восстановлении оксидов кобальта углеродом ( коксом, древесным углем) получают металлический кобальт, загрязненный углеродом или карбидами кобальта. Сырой кобальт очищают плавлением в высоком вакууме, методом зонной плавки или электролитическим рафинированием. [26]
Нестойкий кубический кобальт был идентифицирован как продукт восстановления стандартных кобальтовых катализаторов, тогда как гексагональный кобальт был найден в продуктах гидрирования карбида кобальта. В отработанных кобальтовых катализаторах рентгенографическим исследованием карбид обнаружен не был. Объемная фаза карбида снижает активность кобальтовых катализаторов. Результаты измерения величины поверхности указывают на то, что при превращении кобальта в кобальтовых катализаторах в карбид кобальта заметного изменения величины поверхности не происходит. Науглероживание в условиях образования свободного углерода значительно увеличивает поверхность. [27]
В дальнейшем применение радиоактивного изотопа углерода С14 для распознавания образования карбидов на кобальтовом катализаторе показало, что при температуре 200 только около 10 % углеводородов образуется через карбид кобальта, а вся основная масса продуктов образуется, минуя стадию образования карбида кобальта как промежуточного продукта. [28]
Следовательно, наши советские ученые Я. Т. Эйдус и Н. Д. Зелинский первыми доказали, что при синтезе жидких углеводоро - Ч дов из окиси углерода и водорода над кобальтовыми и никеле-катализаторами карбиды кобальта и никеля не являются ни промежуточными продуктами, ни катализаторами реакции синтеза. [29]
В дальнейшем применение недавно открытого радиоактивного изотопа углерода С14 для распознавания образования карбидов на кобальтовом катализаторе показало, что при температуре 200 С только около 10 % углеводородов образуется через карбид кобальта, а вся основная масса продуктов образуется, минуя стадию образования карбида кобальта как промежуточного продукта. [30]
Страницы: 1 2 3 4