Карбоксилат-ион
Cтраница 3
Согласно рентгеноструктурным исследованиям оба атома кислорода в карбоксилат-ионе находятся на одинаковом расстоянии от углерода. [31]
Из чего же следует, что в карбоксилат-ионе действительно имеет место делокализация я-электронов. [32]
В ряде комплексов, где X представляет собой карбоксилат-ион, существует не только корреляция более высоких скоростей с более низкой основностью RCOO - групп, но и отсутствует какое-либо снижение констант, обусловленное возрастающими размерами R, помимо того, которое вытекает из влияния основности. При 5н2 - механизме возросшие размеры R должны вызвать уменьшение скорости, по меньшей мере в том случае, если атака происходит с той стороны, где расположена группа, хотя не исключена возможность атаки с противоположной стороны. [33]
Ангидриды получают или замещением хлора в хлорангидриде кислоты на карбоксилат-ион или нагреванием кислоты с кислым обезвоживающим сметном типа пятиокиси фосфора или уксусного ангидрида. [34]
Благодаря полной делокализации заряда на двух электроотрицательных атомах кислорода карбоксилат-ион обладает довольно высокой стабильностью. Поэтому карбоновые кислоты значительно превосходят по кислотности спирты и фенолы. [35]
Ангидриды получают или замещением хлора в хлорапгидриде кислоты на карбоксилат-ион или нагреванием кислоты с кислым обезвоживающим агентом типа пятиокиси фосфора или уксусного ангидрида. [36]
В противоположность этому для большого числа случаев например для карбоксилат-ионов и протонированных аминов было показано, что вклад эффекта электрического поля в экра. Конечно, изменения До зг счет поляризации связей являются бесспорным следствием изменений 0пара и адиа, & качественная оценка эффекта электрического поля с помощью классических уравнений, подобные уравнению ( IV. Аналогично и эффект вандерваальсовых взаимодействий, который, по всей вероятности, связан с - эффектом, обсуждаемым ниже, можно трактовать с позиций моделей поляризации связи. [37]
Рентгеноструктурные исследования показали, что оба атома кислорода в карбоксилат-ионе находятся на одинаковом расстоянии от углерода. [38]
Данные физических измерений также указывают на делокализацию заряда в карбоксилат-ионе. В формиат-ионе обе С-О связи равны по длине и длина этой связи 1.27 А оказывается промежуточной между СО связью ( 1.20 А) и С-О ( 1.34 А) в самой муравьиной кислоте. [39]
Схемы (10.7) и (10.8) показывают примеры электрофильно-нук-леофильных механизмов, где карбоксилат-ион в орго-положении реагирует с протонированным субстратом, давая промежуточные соединения, которые затем превращаются в продукты. Постулируемый на схеме (10.7) промежуточный продукт в условиях реакции достаточно стабилен; что же касается промежуточного продукта на схеме (10.8), то скорость его превращения в продукты выше общей скорости реакции. [40]
Схемы (10.7) и (10.8) показывают примеры электрофильно-нук-леофильных механизмов, где карбоксилат-ион в орго-положении реагирует с протонированным субстратом, давая промежуточные соединения, которые затем превращаются в продукты. Постулируемый на схеме (10.7) промежуточный продукт в условиях реакции достаточно стабилен; что же касается промежуточного продукта на схеме (10.8), то скорость его превращения в продукты выше общей скорости реакции. [41]
Свободный карбоксильный радикал ( ацилоксил) декарбоксили-руется легче, чем карбоксилат-ион. [42]
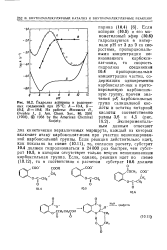 |
Гидролиз аспирина и родствен-ных соединений при 25 С. Л -, Б -, Я-10. 6. Из работы. Morawetz Н., Oreskes L, J. Am. Chem. Soc., 80, 2591 ( 1958. 1958 by the American Chemical Society. [43] |
Два кинетически неразличимых маршрута, каждый из которых включает атаку карбоксилат-иона при участии неионизированной карбоксильной группы. Если реакция действительно идет, как показано на схеме (10.11), то, согласно расчету, субстрат 10.4 должен гидролизоваться в 24000 раз быстрее, чем субстрат 10.5, в котором отсутствует только вторая неионизованная карбоксильная группа. [44]
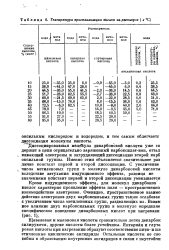 |
Температура кристаллизации кислот из растворов ( в С. [45] |
Страницы: 1 2 3 4