Карбоксипептидаза
Cтраница 1
Карбоксипептидаза освобождает С-концевую аминокислоту, но только в том случае, если имеется подходящая предшествующая аминокислота. [1]
 |
Определение степени рацемизации синтетического Asp - p - амида Уа15 - ангиотензина II ферментативными методами ( Риникер и Швицер. [2] |
Карбоксипептидаза отщепила только С-концевой остаток фенилаланина, а лейцинаминопеп-тидаза ( свободная от пролидазы) - первые пять аминокислот. [3]
Карбоксипептидаза практически нерастворима в воде и в разведенных солевых растворах. Перед использованием суспензию фермента промывают 3 или 4 раза ледяной водой. Неактивный белок, который выпадает в осадок, если оставить раствор на 2 час при 4, отделяют центрифугированием на холоду. [4]
 |
Определение степени рацемизации синтетического Asp - p - амида Уа15 - ангиотензина II ферментативными методами ( Риникер и Швицер. [5] |
Карбоксипептидаза отщепила только С-концевой остаток фенилаланина, а лейцинаминопеп-тидаза ( свободная от пролидазы) - первые пять аминокислот. [6]
Карбоксипептидаза А вырабатывается ацинарными клетками поджелудочной железы в виде неактивного профермента. [7]
 |
Две возможные роли остатка Glu-270 при гидролизе. основной катализ атаки водой ( а и образование промежуточного ангидрида ( б. [8] |
Карбоксипептидаза А и другие пептидазы. [9]
Карбоксипептидаза отщепляет аминокислоту со стороны свободной карбоксильной группы. Разрыв происходит по месту первой пептидной связи от этого конца цепи, особенно если остаток связанной пептидной связью аминокислоты будет радикалом тирозина или фенилаланина. Присутствие свободной аминной группы мешает действию фермента. [10]
Карбоксипептидаза содержится в поджелудочной железе высших животных. Выделена она в кристаллической форме. [11]
Карбоксипептидаза также обусловливает превращение белков, в результате которого образуются растворимые соединения без заметного изменения молекулярного веса, а иногда и без потери биологической активности. Карбоксипептидаза способна выделять аминокислоты из некоторых белковых субстратов, воздействуя главным образом на С-концевые положения, которые соответствуют ее специфическим структурным требованиям. В течение последних двух лет Карбоксипептидаза исследовалась как возможный общий реагент, пригодный для осуществления контролируемого постепенного расщепления белков и для идентификации С-концевых аминокислот. Этот вопрос рассмотрен в статьях II и III, однако не следует недооценивать преимуществ применения карбоксипептидазы и в исследованиях изменения белков под действием ферментов. [12]
Карбоксипептидаза катализирует отщепление С-концевой аминокислоты от пептидной цепи, причем наиболее эффективно отщепляются кислоты, содержащие гидрофобные ароматические остатки. [13]
Карбоксипептидаза - это металлофермент, содержащий один атом цинка на молекулу белка. Карбоксипептидаза катализирует гидролиз С-концевой пептидной связи в белках и олигопеп-тидах и сложных эфиров а-оксикислот. По данным рентгеноструктурного анализа Карбоксипептидаза представляет собой глобулярный белок, в котором содержится один атом цинка, координированный двумя остатками гистидина. Кроме того, в состав активного центра входят карбоксильная ( Glu-270), фенольная ( Туг-248) и гуанидиновая ( Arg-145) группы. [14]
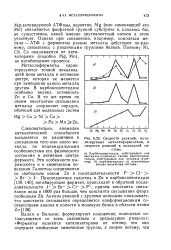 |
Скорости реакций, катализируемых металлоферментами, и скорости реакций в модельной системе. [15] |
Страницы: 1 2 3 4