Карбоксипептидаза
Cтраница 3
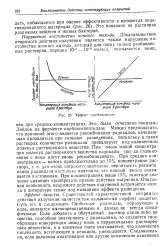 |
Эффект разбавления. [31] |
Это было отчетливо показано Дейлам а ферменте карбоксипептидазе. Можно предполагать, что причиной этого является рекомбинация радикалов, начинающая проявляться при сильных разведениях, поскольку в таких растворах количество радикалов превалирует над количеством молекул растворенного вещества. При очень малой концентрации молекул растворенного вещества радикалы еще до столкновения с ними могут вновь рекомбинировать. При концентрациях выше 15 % заметное значение начинает приобретать прямое действие излучения. Описанная особенность непрямого действия излучений встречается иногда в литературе также под названием эффекта разведения. [32]
Об использовании экзопептидаз, таких как аминопептидаза и карбоксипептидаза, для определения аминокислотной последовательности вблизи N - и С-концов белков говорилось в разд. Эндопептидазы являются протеолитическими ферментами, которые избирательно расщепляют пептидные связи в точках, удален ных от концов белковой молекулы. Эндопептидазы сильно различаются по своей специфичности. Обычно сами аминокислотные остатки с любой стороны расщепляющейся пептидной связи являются наиболее важными детерминантами специфичности про-теолитических ферментов. [33]
Анализируя полную кинетическую кривую гидролиза гип-пурилфенилглицина, катализируемого карбоксипептидазой, авторы [7] получили отрицательные значения & Кат и / Ст ( каяо - Дать объяснение полученным результатам. [34]
Опыты показали, что защитное действие ( с карбоксипептидазой в качестве индикатора) некоторых веществ ( глюкоза, тиомочевина, муравышоки-слый натрий, диметилтиомочевина) понижается с повышением концентрации растворенного вещества. Это явление изменения частного толковалось в том смысле, что, хотя молекулы защитного вещества способны удалять свободные радикалы, они остаются в активном состоянии и могут в свою очередь инактивировать молекулы индикатора. [35]
В соке поджелудочной железы содержатся трипсин, химотрипсин и карбоксипептидаза. [36]
Иллюстрацией такого рода механизмам могут служить реакции, катализируемые карбоксипептидазой А. [37]
При частичном гидролизе гормона роста химотрипсином, трипсином или карбоксипептидазой биологическая активность, по-видимому, не меняется. Гидролиз химотрипсином на 25 % ( превращение белкового азота в небелковый на 25 %) и трипсином на 30 % не ведет к уменьшению биологической активности. Это указывает на то, что сохранение структуры всей белковой молекулы в целом, по-видимому, несущественно для проявления биологической активности гормона роста. [38]
О - ( бензоилглицин) - 2-оксиизовалериановой кислоты, катализируемой карбоксипептидазой А, от концентрации субстрата. [39]
Из рассмотрения формул субстратов, на которые действуют трипсин и карбоксипептидаза ( см. выше), очевидно, что действие этих ферментов зависит главным образом от стереохимической конфигурации молекулярных групп субстрата, от их формы и от их взаимного расположения. Химическая природа расщепляемых связей имеет, повидимому, второстепенное значение. Эта точка зрения хорошо согласуется с утверждением, что соединение фермента с субстратом происходит посредством связей, возникающих между их поверхностями, форма которых соответствует друг другу. [40]
Наиболее известным металлоферментом, катализирующим гидролиз пептидной связи, является карбоксипептидаза. [41]
Реакция происходит в полостях и карманах на гидрофильной поверхности глобулы белка карбоксипептидазы, тогда как все гидрофобные группы спрятаны внутри глобулы, так как их контакт с Н2О, находящейся на поверхности белковой глобулы, энергетически не выгоден. [42]
Влияние н-бутанола на кинетику гидролиза гиппурового эфира L-аргинина, катализируемого карбоксипептидазой В. [43]
Электростатическое взаимодействие фермент-субстрат играет положительную роль также и в катализе карбоксипептидазой А, которая специфически отщепляет аминокислоты от С-конца пептидов и полипептидных цепей белков. Заряженная карбоксильная группа концевого аминокислотного остатка при образовании комплекса Михаэлиса электростатически взаимодействует с положительно заряженной гуа-нидиновой группой Arg-145 ( см. схему на стр. [44]
Влияние н-бутанола на кинетику гидролиза гиппурового эфира L-аргинина, катализируемого карбоксипептидазой В. [45]
Страницы: 1 2 3 4