Кератин - шерсть
Cтраница 1
Кератин шерсти и волос имеет в качестве основного структурного элемента а-спиральные полипептидные цепи, стабилизированные водородными связями и межспиральными дисульфидными мостиками. Аминокислотный состав этого а-кератина обнаруживает высокое ( 11 %) содержание цистеи-на и гидрофобных аминокислот. [1]
Восстановители разрушают кератин шерсти, восстанавливая цистиновые связи; особенно быстро эта реакция проходит в щелочной среде. [2]
Химическая активность кератина шерсти в значительной степени обусловлена присутствием цистина который легко поддается окислению. [3]
Если молекулу кератина шерсти растянуть, то извитая конфигурация перейдет в линейную ( р-модификация кератина), при этом остается слабовыраженная извитость, вызываемая характером валентных углов и межмолекулярными расстояниями. [4]
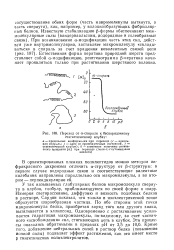 |
Переход от а-спирали к беспорядочному статистическому клубку. [5] |
Естественная форма кератина природной шерсти представляет собой а-модификацию, рентгенограмма р-кератина начинает проявляться только при растягивании шерстяного волокна. [6]
Амидные группировки имеются в кератине натуральной шерсти и в фиброине натурального шелка. [7]
Метилмеркаптан CH3SH образуется при гидролизе кератина шерсти и гниении белковых веществ, содержащих серу. Он находится также в человеческих испражнениях, являясь вместе со скатолом ( см. том II) причиной их неприятного запаха. [8]
Метилмеркашан CH3SH образуется при гидролизе кератина шерсти и гниении белковых веществ, содержащих серу. Он находится также в человеческих испражнениях, являясь вместе со скатолом ( см. том II) причиной их неприятного запаха. [9]
Присутствие цистиновой связи характерно только для кератина шерсти, а солевой - как для кератина, так и для фиброина. Однако содержание солевых связей в фиброине невелико. [10]
Помимо химической солевой связи, между макромолекулами кератина шерсти имеется химическая ковалентная связь. Возникновение ее связано с тем, что одна из аминокислот одновременно участвует в образовании двух полипептидных цепей. [11]
Большое разнообразие реакционноспособных боковых групп позволяет модифицировать свойства кератина шерсти химическими методами. В то же время эти группы обусловливают многие недостатки шерсти, особенно ее чувствительность к термическому обесцвечиванию, фотохимической деструкции и действию даже слабощелочных реагентов. Большинство химических свойств шерсти связано с наличием в ней дисульфидных цисти-новых мостиков. [12]
В заключение несколько слов еще о важнейшем волокнистом белке - кератине шерсти. Общеизвестна замечательная способность кератинового волокна растягиваться на 120 % во влажной атмосфере. Эстбюри предполагал, что полипептидные цепи кератина могут давать складки и спрямление этих складок объясняет наблюденный им переход. В настоящее время структуры, предполагавшиеся Эстбюрп, имеют лишь исторический интерес. [13]
Моррисон и сотрудники [33] измерили зависимость теплоты смачивания фиброина шелка и кератина шерсти в воде в зависимости от ее содержания в этих веществах. Их данные были хорошо обработаны при использовании термодинамических методов, но было сделано одно допущение о равенстве теплот растворения нулю. Возможно, что эффекты растворения отсутствуют или малы, если теплоты погружения образцов, выдержанных до равновесия вблизи давления насыщения воды, равны нулю. [14]
Синтетические молеядовитые препараты должны обладать следующими свойствами: а) сообщать кератину шерсти полную моле-устойчивость; б) не повреждать волокна шерсти и не влиять на последующие процессы ее отделки; в) быть устойчивыми к стирке, свету и трению; г) обладать полной безвредностью для людей; д) быть простыми в применении, недорогими и негигроскопичными. [15]
Страницы: 1 2 3 4