Кератин - шерсть
Cтраница 2
В умерен-нокислой среде ( рН 4 5 - 5) в кератине шерсти всегда имеется некоторое число незаряженных аминогрупп, которые и принимают участие в этих реакциях. [16]
Он стоек к мокрым обработкам, светопого-де и отличается высоким сродством к кератину шерсти. [17]
Ковалентная связь активного красителя с волокном может образоваться с участием гидроксильных групп целлюлозы или аминогрупп кератина шерсти и полиамидных волокон. Таким образом, активные красители должны содержать группировки, способные связываться с гидроксильными и аминогруппами. [18]
Амидные группировки содержатся также в природных высокомолекулярных веществах, из которых строятся природные волокна - в кератине шерсти и в фиброине натурального шелка. [19]
В красильной ванне происходит отщепление сульфатной группы красителя с образованием активной винилсульфоновой группы, которая реагирует с аминогруппой кератина шерсти. [20]
Две молекулы моноазокрасителя насыщают 4 из 6 координационных связей хрома; две остальные связывают NH2, ОН и другие группы кератина шерсти, повышая устойчивость окрасок. [21]
Количество тирозина в фиброине шелка, в зависимости от сорта последнего, составляет 9 2 - 12 8 %, а в кератине шерсти и казеине - 6 0 % и, по-видимому, в значительной степени определяет относительно высокую светочувствительность этих материалов. [22]
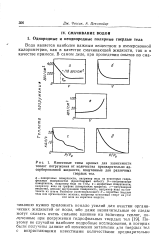 |
Известные типы кривых для зависимости теплот погружения от количества предварительно адсорбированной жидкости, полученные для различных твердых тел. [23] |
Вайоминг ( монтмориллонит); д - пористые твердые тела или органические волокна, например метиловый спирт на угле или вода на кератине шерсти. [24]
Количество тирозина в фиброине шелка, в зависимости от сорта последнего, составляет 9 2 - 12 8 %, а в кератине шерсти и казеине - 6 0 % и, по-видимому, в значительной степени определяет относительно высокую светочувствительность этих материалов. [25]
В связи с тем, что хром в молекулах красителей КМК 1: 2 полностью координационно насыщен, он не может образовать с кератином шерсти координационных связей. [26]
Волокно шелка менее стойко к горячей воде, чем шерстяное, так как составные части шелка - серицин и фиброин легче гидролизуются, чем кератин шерсти. Как все белковые вещества, шелк значительно набухает за счет интермицелярного проникновения воды. [27]
Это ясно видно на примере двух белков - яичного альбумина и р-лактоглобулина, у которых аминокислотный состав приблизительно одинаков, а также на примере инсулина и кератина шерсти. Различная растворимость этих белков показывает, как сильно зависят свойства белков от распределения боковых ( полярных и неполярных) групп в пептидной цепи. Действительно, известно, что растворимость альбуминов и глобулинов целиком определяется взаимным расположением ионных групп. [28]
Белковые вещества классифицируются также по форме их молекул: а) фибриллярные ( волокнистые) белки, молекулы которых имеют нитевидную форму; к ним относят фиброин шелка, кератин шерсти; б) глобулярные белки, молекулы которых имеют округлую форму; к ним относятся, например, альбумины, глобулины и ряд других, в том числе и сложные белки. [29]
В этих продуктах полиметиленовые цепочки ( СН2) 4 и 6 связаны амидными группировками NH-СО -, содержащимися также в полипептидах, в природных веществах белкового характера: в кератине шерсти и в фиброине шелка. [30]
Страницы: 1 2 3 4