Кинетика - ферментативная реакция
Cтраница 1
 |
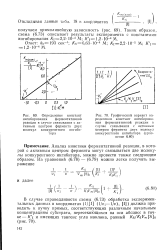
Зависимость скорости ферментативной реакции от количества фермента. [1] |
Кинетика ферментативных реакций изучает скорость биохимических реакций, которые протекают в присутствии катализаторов - ферментов. Живые клетки способны проводить очень быстро сложные реакции при температуре 37 и ниже. [2]
Кинетика ферментативных реакций, разработанная Михаэлисом и Ментен на основе реакций первого порядка, применима к гидролитическим реакциям, так как концентрация воды практически постоянна и гидролитические реакции можно рассматривать как псевдомономолекулярные. [3]
Кинетика ферментативных реакций как метод изучения механизма действия индивидуальных ферментов и систем ферментов все больше привлекает внимание исследователей. Использовать принципы химической кинетики применительно к реакциям, катализируемым ферментами, начали уже довольно давно - много десятилетий назад. Однако по мере того, как становилось ясно, что механизм ферментативных реакций значительно сложнее механизма самых сложных небиологических реакций, ценность измеряемых экспериментально кинетических констант подвергалась все большему сомнению. Это в свою очередь служило мощным стимулом для совершенствования теории и методов самой ферментативной кинетики. В результате эта наука сейчас достигла несомненных успехов, позволяющих достаточно плодотворно применять ее при изучении механизмов ферментативного катализа. Именно по этим причинам ни одна книга по ферментам не обходится сейчас Ч5ез глав по кинетике, хотя эти вопросы излагаются обычно достаточно кратко. [4]
Кинетика ферментативных реакций в предстационарном режиме их протекания изучается в основном методами остановленной струи. Принципиальная особенность этих методов состоит в быстром смешивании растворов реагирующих веществ в смесительной камере специальной конструкции [3, 4], после чего смесь поступает в измерительную кювету. Чаще всего в установках типа остановленной струи используется спектрофотометрический метод измерения с осциллографической регистрацией сигнала от фотоумножителя. Мертвое время лучших современных установок подобного типа составляет 0 1 - 0 3 мсек. [5]
Кинетика ферментативных реакций в предстационарном режиме их протекания изучается в основном методами остановленной струи. Принципиальная особенность этих методов состоит в быстром смешивании растворов реагирующих веществ в смесительной ка мере специальной конструкции [3, 4], после чего смесь поступает в измерительную кювету. Чаще всего в установках типа остановленной струи используется спектрофотометрический метод измерения с осциллографической регистрацией сигнала от фотоумножителя. Мертвое время лучших современных установок подобного типа составляет 0 1 - 0 3 мсек. [6]
 |
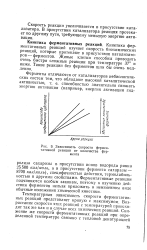
Принцип фермент-субстратного контакта.| Фермент-субстратный комплекс ( пептидаза. [7] |
Исследования кинетики ферментативных реакций выявили, что некоторые ферменты должны обладать ионами металлов для соединения фермента с субстратом, а для других ферментов металлы являются основным компонентом активного центра. [8]
Анализ кинетики ферментативной реакции, в которой с активным центром фермента могут связываться две молекулы конкурентного ингибитора, можно провести также следующим образом. [10]
Анализ кинетики ферментативной реакции (6.35) может быть проведен также следующим образом. [11]
Анализ кинетики ферментативной реакции, в которой с активным центром фермента могут связываться две молекулы конкурентного ингибитора, можно провести также следующим образом. [13]
Возникновение кинетики ферментативных реакций, которое, кстати, произошло задолго до того, как какой-либо из чистых ферментов стал доступен химическому изучению, окончательно прояснило то обстоятельство, что процесс ферментативного катализа зависит от соединения фермента с субстратом. В основе этих представлений лежала общая идея, что соединение с ферментом вызывает известного рода активацию молекулы субстрата. [14]
При рассмотрении кинетики ферментативных реакций и кинетики этих реакций в присутствии ингибиторов предполагалось, что активные центры ферментов ведут себя независимо друг от друга. Это справедливо в тех случаях, когда молекула фермента имеет бдин активный центр. [15]
Страницы: 1 2 3 4