Кинетика - ферментативная реакция
Cтраница 3
Как мы уже видели при рассмотрении кинетики ферментативной реакции, одним из факторов, определяющих ее скорость, является количество доступного субстрата. Однако еще чаще скорости ферментативных процессов регулируются концентрациями различных кофакторов. Различные кофакторы и подобные им по функции метаболиты-переносчики, являющиеся общими для нескольких ферментных систем, могут выполнять важную функцию регуляции и интеграции процессов обмена. [31]
Данное уравнение, являющееся основным уравнением кинетики ферментативных реакций, носит название уравнения Михаэлиса - Ментен. [32]
При наличии в сточных водах токсичных веществ кинетика ферментативных реакций может существенно отличаться от кинетики по классическому уравнению Михаэлиса - Ментен. Причиной снижения скорости реакций в присутствии ингибирующих веществ является взаимодействие ингибитора с ферментом. [33]
 |
Проверка уравнения Михаэлиса для.| Неприменимость уравнения Михаэлиса. [34] |
Уравнение вида (XII.33) или (XII.34) носит в кинетике ферментативных реакций название уравнения Михаэлиса. Впервые оно было применено к инверсии тростникового сахара ( сахарозы) ферментом сахаразой, извлекаемой из дрожжей; далее было показано, что ему подчиняется вообще гидролиз эфиров эстеразами - а также некоторые другие ферментативные реакции. [35]
За работой Таммана последовали другие, посвященные изучению кинетики ферментативных реакций. [36]
 |
Изменение внутренней, энергии реаги jj.| Последовательное окисление веществ. [37] |
Процесс потребления органического вещества из сточных вод определяется кинетикой ферментативных реакций, протекающих внутри клетки. При этом общая скорость протекания биохимических реакций, осуществляющихся внутри клетки, определяется течением самой медленной реакции. Рассмотрим механизм такой реакции. [38]
Описанный в задаче эксперимент - один из вариантов интегрального анализа кинетики ферментативных реакций. [39]
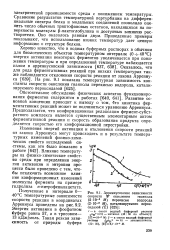 |
Аррениусовские зависимости скорости W окисления гваякола ( 2 - Ю-3 М перекисью водорода ( 2 - 10 - М, катализируемого пероксидазой ( Е. [40] |
Развитие основной концепции приводит к выводу о том, 4 то кинетика ферментативных реакций может не подчиняться уравнению Аррениуса. Предполагается, что конформационная релаксация фермент-субстратного комплекса является существенным элементарным актом ферментативной реакции и скорость образования продукта определяется скоростью его конформационной перестройки. [41]
Уонг [11] недавно также рассмотрел вопросы, связанные с математическим описанием кинетики ферментативных реакций, обратив особое внимание на гипотезу стационарности. Он отмечает, что существенным условием применимости гипотезы стационарности является быстрое образование фермент-субстратного комплекса - условие, которое, несомненно, выполняется при достаточно большом избытке субстрата по отношению к ферменту. [42]
Работы по очистке и выделению ферментных препаратов проводились параллельно с изучением кинетики ферментативных реакций и созданием, как мы только что видели, первых теорий механизма действия ферментов. Что же касается значения первых попыток очистки и концентрации ферментных препаратов, то следует обратить внимание на следующие обстоятельства. [43]
Второй этап, начавшийся с исследований Фишера, работ по созданию кинетики ферментативных реакций и работ по выделению и очистке ферментных препаратов, продолжался до начала 50 - х годов. [44]
Необходимо рассмотреть еще один частный случай, нередко встречающийся в практике исследования кинетики ферментативных реакций. Речь идет о процессах, скорость которых в пределах времени наблюдения остается постоянной. Такая ситуация может возникнуть в случае избытка одного компонента по отношению к другому ( для бимолекулярных реакций) и незначительной глубины реакции в течение времени наблюдения. [45]
Страницы: 1 2 3 4