Кинетика - взаимодействие
Cтраница 1
Кинетика взаимодействия окислов титана и ниобия с хлоралюминатом натрия в расплаве. [1]
Кинетика взаимодействия в системе Ж - Т рассматривается на примере процессов растворения и выщелачивания. Обычно процессы растворения идут в диффузионной или переходной области. При физическом обратимом растворении разрушается кристаллическая решетка и частицы твердого вещества переходят в раствор. [2]
Кинетика взаимодействия между n - хлорфенилизоцианатом и метиловым спиртом в к-гептане. [3]
Кинетика взаимодействия в системе Ж - Т рассмотрена на примере процессов растворения и выщелачивания. Обычно процессы растворения идут в диффузионной или переходной области. При физическом обратимом растворении происходит разрушение кристаллической решетки и переход частиц твердого вещества в раствор. [4]
Кинетика взаимодействия некоторых титановых силавок с водородом при 6ГО С и давлениях до НЮ м гт.сг. бкдя изучена вг. [5]
Кинетика взаимодействия хлора с органическими соединениями, действующие агенты окисления и характеристика конечных продуктов реакции изучены для ограниченного числа объектов. [6]
Кинетика взаимодействия диалкилфосфитов с альдегидами изучена мало [1], данные же по кинетике взаимодействия хлорал я с д-и-метилфосфитом вообще отсутствуют. Согласно схеме, рассматриваемой в монографии А. [7]
Кинетика взаимодействия диалкилфосфитов с альдегидами изучена мало J1 ], данные же по кинетике взаимодействия хлораля с ди-метилфосфитом вообще отсутствуют. Согласно схеме, рассматриваемой в монографии А. [8]
Кинетика взаимодействия алканов с SO2 в присутствии кислорода и промоторов ( с промежуточным образованием надсульфоновых кислот) или в присутствии кислорода, промоторов и воды изучена недостаточно. Более подробно изучена кинетика сульфирования ароматических соединений. [9]
Кинетика взаимодействия фенил-р-цианвинилкетона с метиловым спиртом исследована нами спектрофотометрическим методом. На рис. 1 приведены УФ-спектры обоих геометрических изомеров фенил-р-цианвинил-кетона и продукта реакции фенил-р-метокси-р - цианэтилкетона. Реакция протекает обратимо, причем равновесие сильно сдвинуто в сторону продукта присоединения. К одной и той же реакционной смеси можно прийти с обеих сторон, исходя как из цис - и игранс-изомеров фенил-р-цианвинилкетона, так и из фенил-р-метокси-р - цианэтилкетона. Положение равновесия практически не зависит от рН раствора. Так, один и тот же спектр конечной реакционной смеси получен как в присутствии метилата натрия различной концентрации, так и в ацетатном буфере, причем прибавление кислоты не приводит к его изменению. [10]
Кинетика взаимодействия молибдена с вадшшм жаром при Т; 1100 С описывается урашшием прямой. Кинетика процесса описывается уравнением прямой. С соответственно, В среде азота при высоких температурах стабильные нитриды образуют следующие техшгчешш шащные щеталлБг ( перечислены в порядке уменьшения энергии связи металл - азот): Hf, Zr, Ti, A1, Та, Mb, Cr. Скорость азотирования, как правило, - ниже скорости взаимодействия с кислородом. Металлы IV-a группы медленно взаимодействуют с азотом. Процесс описывается уравнением параболы. Ниобий и тантал взаимодействуют с азотом по параболическому временному закону. [11]
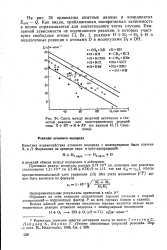 |
Связь между энергией активации и теплотой реакции для экзотермических реакций типа X RY - R XY ( по данным Н. Н. Семенова. [12] |
Кинетика взаимодействия атомного водорода с молекулярным была изучена А. [13]
Кинетика взаимодействия монодисперсных порошков также не всегда от начала и до конца протекания реакции описывается одним и тем же уравнением. Причин здесь несколько, и они не обязательно обусловлены сменой механизма твердофазных взаимодействий. [14]
Кинетика взаимодействия монодисперсных порошков также не всегда от начала и до конца описывается одним и тем же уравнением. Причин здесь может быть несколько, и они не обязательно обусловлены сменой механизма взаимодействия. [15]
Страницы: 1 2 3 4