Кинетика - взаимодействие
Cтраница 3
Изучена кинетика взаимодействия сульфида кальция с раствором хлорида аммония по степени разложения NH4CI в растворе в интервале 20 - 95 С. [31]
Поскольку кинетика взаимодействия алкиламмониевых катионов с различными солевыми формами глинистых минералов практически не изучалась, мы поставили своей целью выяснение этого вопроса. В данной работе изучена кинетика обмена ионов Na, Ca2, Ni2, Al3 монтмориллонита с растворами бутиламмонийхлорида. В качестве объекта исследования был взят монтмориллонит Пыжевского месторождения. [32]
Изучению кинетики взаимодействия мочевины с формальдегидом полярографическим методом посвящена также работа Лойда и Смита [12], причем полярографический метод определения концентрации формальдегида, рассмотренный в этой работе, впоследствии нашел применение для анализа производственных конденсатов. [33]
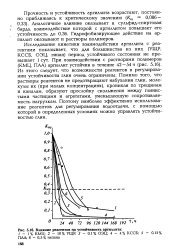 |
Влияние реагентов на устойчивость аргиллита. [34] |
Исследование кинетики взаимодействия аргиллита с реагентами показывает, что для большинства из них ( УЩР, КССБ, ОЭЦ, гипан) период устойчивого состояния не превышает 1 сут. Из этого следует, что возможности реагентов в регулировании устойчивости глин очень ограничены. Помимо того, что растворы реагентов не предотвращают набухания глин, молекулы их ( при малых концентрациях), проникая по трещинам и каналам, образуют прослойку скольжения между глинистыми частицами и агрегатами, уменьшающую сопротивляемость нагрузкам. Поэтому наиболее эффективно использование реагентов для регулирования водоотдачи, с помощью которой в определенных условиях можно управлять устойчивостью глин. [35]
Изучение кинетики взаимодействия ряда катионов - Sc3, Ybs, РгЗ, Tm3, La3, Y3 с меркаптоэтиламин - N, N, S-триуксусной кислотой показало, что изотермы проводимости в момент приготовления растворов, а также яерез один час и одни сутки аналогичны. На основании этого был сделан вывод о сравнительно быстром образовании достаточно прочных комплексов меркаптоэтиламин - N, N, S-триуксусной кислоты с этими металлами. [37]
Изучение кинетики взаимодействия перекиси бензоила с вторичными ароматическими аминами методом полимеризации и реакции с дифенилпикрилгидразином показало [612], что реакции анилина и дифениламина с перекисью бензоила, хотя и приводят к образованию радикалов, однако не являются цепными. [38]
Исследования кинетики взаимодействия закисного железа с кислородом в сточной воде девонских месторождений показали ( рис. 12), что в нейтральных электролитах ( рН5 2 - 6 2) скорость реакции незначительна. Скорость этой реакции резко возрастает при подщелачивании среды аммиаком. Так, в сточной воде при рН8 5 реакция при интенсивной аэрации заканчивается-через 15 мин. Если опыт вести при ограниченном доступе кислорода, то при рН 6 0 через 1 сут остается еще 70 % непрореагировавшего кислорода. [39]
Изучение кинетики взаимодействия ряда катионов - Scs, Yb3, Pr3, Тт3, La3, Y3 с меркаптоэтиламин - N, N, S-триуксусной кислотой показало, что изотермы проводимости в момент приготовления растворов, а также яерез один час и одни сутки аналогичны. На основании этого был сделан вывод о сравнительно быстром образовании достаточно прочных комплексов меркаптоэтиламин - N, N, S-триуксусной кислоты с этими металлами. [41]
Изучение кинетики взаимодействия эфиров фосфористой кислоты с гидроперекисями показало, что скорость реакции в данном случае находится в обратной связи с ингибирующеи способностью фосфитов. [42]
Изучение кинетики взаимодействия первичных и третичных амчнов с серной кислотой подтверждает промежуточное образование арилг. [43]
 |
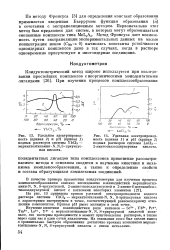
Зависимость скорости взаимодействия NH3 с Ka [ PtCl4 ] от концентрации NH3.| Зависимость скорости взаимодействия NH3 с K [ PtNH3Cl3 ] от концентрации NH3. [44] |
Изучая кинетику взаимодействия хлороплатинита калия и соли Косса с аммиаком, нам удалось показать [ 97J, что коэффициент скорости замещения одного из хлоров в K2 [ PtCl4 ] на аммиак примерно в 2.5 раза меньше коэффициента скорости замещения атома хлора в соли Косса. [45]
Страницы: 1 2 3 4