Кинетика - выделение - водород
Cтраница 2
Влияние различных примесей на кинетику выделения водорода на амальгамном электроде в большой степени зависит от экспозиции. [16]
Количественно оценить действие различных примесей в рассоле на кинетику выделения водорода в ртутном электролизере весьма затруднительно. Лабораторные опыты недостаточно воспроизводимы, отклонения полученных результатов достигают 30 %, а иногда наблюдаются и качественные расхождения. [17]
При этом к растворителю предъявляются два требования - во-первых, кинетика выделения водорода из него должна существенно отличаться по своим количественным параметрам от кинетики его выделения из водных растворов с тем, чтобы можно было достаточно четко сопоставлять и различать эти два процесса; во-вторых, основность растворителя должна быть значительно меньше, чем воды, что позволяет с помощью малых добавок воды перевести практически все ионы водорода из формы сольвониевого иона в гидроксоний. В качестве растворителя, удовлетворяющего этим требованиям, был выбран слабоосновный апротонный растворитель - аце-тонитрил. [18]
Полученный нами на ряде металлов экспериментальный материал показывает, что кинетика выделения водорода в широкой области потенциалов не может быть описана на основании представления о замедленности только одной из возможных стадий суммарного процесса. Механизм перенапряжения на металлах, адсорбирующих водород, особенно в щелочных растворах, более сложен. Для полного описания его необходимо учитывать две, а возможно, и большее число стадий, которые в определенных областях поляризации протекают с соизмеримыми скоростями. [19]
Пленка окалины, полученная окислением при 700 С, меняет и кинетику выделения водорода. [21]
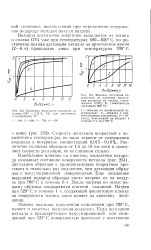
В табл. 3, 4 и 5 приведены результаты опытов по кинетике выделения водорода из титана, ниобия и тантала после их предварительного насыщения водородом до равновесного содержания при давлении 10 - 4 торр. [22]
К настоящему времени имеется большое число исследований, посвященных влиянию примесей на кинетику выделения водорода в процессах электролиза с ртутным катодом. Иногда наблюдаются и качественные расхождения. Однако имеются общие и не вызывающие сомнений закономерности. В первую очередь к ним относятся следующие. [23]
Указанная классификация позволила объяснить многочисленные экспериментальные данные различных авторов, полученные при исследовании кинетики выделения водорода из осадков. Наличие молекулярного водорода в электролитических осадках считается общепризнанным фактом. [24]
Как уже отмечалось, скорость коррозии металлов в кислых средах чаще всего определяется кинетикой выделения водорода. Ингибиторы кислотной коррозии не только тормозят коррозионной процесс в целом, но и могут влиять на соотношение скоростей отдельных стадий выделения водорода. Путем анализа зависимости Екор и lg / Kop от рН Л. Н. Антропов убедительно показал [48], что в присутствии органических аминов катодное выделение водорода на железе тормозится на стадии разряда, а в присутствии неионогенного ингибитора - антрани-ловой кислоты - на стадии рекомбинации. [25]
Ко второй группе относятся ртуть, свинец, цинк, кадмий и некоторые другие металлы, на которых кинетику выделения водорода определяет замедленный разряд ионов водорода. Это р-эдементы, у которых нет неспаренных d - электронов, вследствие чего акт раз - ряда иона водорода затруднен. На поверхности этих металлов концентрация атомарного водорода незначительна, поэтому восстановление органических веществ на таких электродных материалах атомарным водородом маловероятно. [26]
Ко второй группе относятся ртуть, свинец, цинк, кадмий и некоторые другие металлы, на которых кинетику выделения водорода определяет замедленный разряд ионов водорода. Это sp - элементы, у которых нет неспаренных - электронов, вследствие чего акт разряда иона водорода затруднен. На поверхности этих металлов концентрация атомарного водорода незначительна, поэтому восстановление органических веществ на таких электродных материалах атомарным водородом маловероятно. [27]
Ко второй группе относятся ртуть, свинец, цинк, кадмий и некоторые другие металлы, на которых кинетику выделения водорода определяет замедленный разряд ионов водорода. Это sp - элементы, у которых нет неспаренных d - электронов, вследствие чего акт разряда иона водорода затруднен. На поверхности этих металлов концентрация атомарного водорода незначительна, поэтому восстановление органических веществ на таких электродных материалах атомарным водородом маловероятно. [28]
Во-первых, потенциал на границе раздела железный катод - раствор электролита определяется активностью водорода в поверхностном слое железа и кинетикой выделения водорода из раствора на поверхности железа. Во-вторых, стимуляторы и ингибиторы наводороживания могут смещать потенциал чистой поверхности железного катода в одну и ту же сторону ( например, увеличивать), оказывая первые - ускоряющее, а вторые - тормозящее влияния на наводороживание металла катода. Поэтому лишь в простейших случаях, когда не происходит никаких изменений состава электролита, физического и химического состояния поверхности катода, не происходит изменения механизма катодного процесса, можно ожидать простой зависимости между, например, потоком диффундирующего через мембрану-катод водорода и потенциалом и поляризуемой стороны мембраны. [29]
Если радикалы Н02 и ОН способны диссоциировать на ионы, то очевидно, что концентрация водородных иопов должна влиять на кинетику выделения водорода при облучении воды. В этой связи кинетика выделения водорода была исследована в растворах H2S04 и КОН, насыщенных кислородом и азотом. [30]
Страницы: 1 2 3 4