Кинетика - выделение - водород
Cтраница 3
Желая изучить природу попавшего в осадок водо рода, а также механизм его попадания, мы провел:, серию опытов, связанных с установлением кинетика выделения водорода в зависимости от температурь: нагрева в вакууме. [31]
Эти общие заключения о природе перенапряжения на разных металлах подтверждаются в общих чертах соответствием между наиболее важными следствиями из теории перенапряжения водорода и данными, полученными при экспериментальном изучении кинетики выделения водорода. Так, на поверхности ртути в области потенциалов катодного выделения водорода ни одним из методов не удается обнаружить заметных следов адсорбированного атомарного водорода. Следовательно, стадия его удаления не является лимитирующей. При учете ничтожно малого заполнения поверхности ртутного катода адсорбированным атомарным водородом такое значение величины b не может быть получено из теории замедленной рекомбинации. Экспериментальные данные по влиянию состава раствора и рН на перенапряжение при выделении водорода на ртути также лучше всего согласуются с предположением о замедленности разряда на свободных участках катода. [32]
Эти общие заключения о природе перенапряжения на разных металлах подтверждаются в общих чертах соответствием между наиболее важными следствиями из теории перенапряжения водорода и данными, полученными при экспериментальном изучении кинетики выделения водорода. Так, на поверхности ртути в области потенциалов катодного выделения водорода ни одним из методов не удается обнаружить заметных следов адсорбированного атомарного водорода. Следовательно, стадия его удаления не является лимитирующей. При учете ничтожно малого заполнения поверхности ртутного катода адсорбированным атомарным водородом такое значение величины Ъ не может быть получено из теории замедленной рекомбинации. Экспериментальные данные по влиянию состава раствора и рН на перенапряжение при выделении водорода на ртути также лучше всего согласуются с предположением о замедленности разряда на свободных участках катода. [33]
При этом общее содержание водорода в литых образцах устанавливалось как при помощи использования метода вакуум-плавления, так параллельно и путем вакуум-нагрева с последующим анализом выделенного газа; кроме того, изучалась кинетика выделения водорода во время хранения литых проб-под ртутью при комнатной температуре. [34]
Стойкость стали к растрескиванию в насыщенном сероводородом 20 % - ном растворе поваренной соли при 261 К возрастает в 10 раз по сравнению с 291 К, что, возможно, объясняется изменением структуры воды и кинетики выделения водорода. Установлено увеличение наводороживания при катодной поляризации полированной стали по сравнению с грубо шлифованной. [35]
В системах с участием энзоменов протекает несколько последовательных процессов: 1) междоменный обмен электронами, 2) перенос электронов на активный центр ( восстановление активного центра), 3) образование продукта восстановленным активным центром фермента. Исследование кинетики выделения водорода после предварительной поляризации матрицы для образцов с различным удельным содержанием активных центров фермента показало, что лимитирует скорость процесса ферментативная стадия. Процессы междоменного обмена и переноса электронов на активные центры фермента протекают существенно быстрее. [36]
Если радикалы Н02 и ОН способны диссоциировать на ионы, то очевидно, что концентрация водородных иопов должна влиять на кинетику выделения водорода при облучении воды. В этой связи кинетика выделения водорода была исследована в растворах H2S04 и КОН, насыщенных кислородом и азотом. [37]
Образование Н202 в воде с растворенным кислородом изучали Фрикке [2, 4, 5] под действием рентгеновских лучей, Лофор [6], под действием ас-частиц и рентгеновских лучей, Джонсон и Аллен, под действием жестких рентгеновских лучей [7 ], Эберт и Боуг [8 ], под действием электронов и рентгеновских лучей, Хоханадель [9], под действием - ( - лучей Со60, и Джонсон [10], под действием рентгеновских лучей с энергией 2 Мэв. В большинстве этих работ кинетика выделения водорода вовсе не изучалась, только в некоторых работах [7, 9, 11] были получены отдельные кинетические данные по выделению водорода из растворов Н202 и 02 при их облучении. [38]
I, на металлах второй группы кинетику выделения водорода определяет замедленный разряд ионов водорода. На поверхности этих металлов концентрация атомарного водорода незначительна, поэтому восстановление органических веществ на таких электродных материалах атомарным водородом маловероятно. [39]
Скорость разряда водорода на амальгаме натрия не зависит от рН раствора, поэтому сведения о трудности выделения водорода на амальгамном электроде вследствие подщелачивания прика-тодного слоя несостоятельны. Возрастание величины рН может влиять на кинетику выделения водорода только в области кислых растворов. [40]
Для металлов первой электрохимической группы, у которых кинетика выделения водорода определяется скоростью химической реакции (36.11), ингибирующее действие добавок будет определяться, в основном, механическим экранированием поверхности и изменением поверхностной концентрации адатомов водорода ( изменением величин 0 и fz ( c) уравнения ( 31)), а электрические свойства частиц должны играть второстепенную роль. [41]
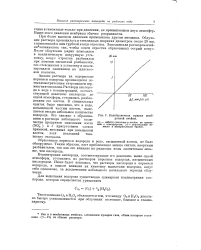 |
Калибровочная кривая мембранной ячейки. [42] |
Концентрации кислорода, соответствующие его давлению выше одной атмосферы, готовились из растворов перекиси водорода, насыщенных кислородом. Ниже будет показано, что растворы кислорода и перекиси водорода, в смысле влияния на кинетику выделения водорода, ведут себя одинаково, за исключением небольшого начального периода облучения. [43]
Из уравнений ( 17), ( 18) ясно, что величина концентрации поглощенного металлом водорода может существенно зависеть от скорости электроосаждения. Однако основное влияние на величину наводороживания металлов оказывает коэффициент проникновения у, величина которого зависит от природы металла и кинетики выделения водорода. Поэтому снижение степени наводороживания основы в процессе нанесения гальванических покрытий может быть достигнуто путем снижения величины этого коэффициента, например введением в раствор соответствующих поверхностноактивных веществ. [44]
Так, избыток адсорбированного водорода повышает емкость двойного электрического слоя и увеличивает перенапряжение. Так как скорость рекомбинации увеличивается параллельно с поверхностной концентрацией водорода, а последняя может расти до известного предела, отвечающего поверхностному насыщению, то для металлов, на которых кинетика выделения водорода определяется рекомбинацией, следует ожидать появления предельной плотности тока недиффузионного происхождения. [45]
Страницы: 1 2 3 4