Кислота - льюис
Cтраница 2
Кислоты Льюиса как катализаторы вызывают реакции сужения и расширения циклов, проходящие через карбениевые ионы, по типу, рассмотренному для изомеризации н-бутана в изобутан. В равновесной смеси циклоалканов обычно преобладают пяти - и шестичленные циклы. Трех -, четырех -, семи-и более высокочленные циклы обычно отсутствуют в равновесных смесях, что находится в согласии с общими соображениями относительно энергии напряжения этих циклов. Так, циклопентан не образует циклопропанов или метилциклобутана, а циклогептан изо-меризуется в метилциклогексан. При обычной температуре в равновесной смеси пяти - и шестичленных циклов преобладают изомеры с большим циклом. Так, в присутствии алюминийгалогенидов при 25 С метилциклопентан и циклогексан образуют равновесную смесь, содержащую 88 % циклогексана. [16]
Кислоты Льюиса катализируют превращение фенилтиоциклопропилмета-нолов в циклобутаноны. [17]
Кислоты Льюиса оказывают также активирующее действие на никель Ренея и никель на кизельгуре. [18]
Кислоты Льюиса образуются в слое отверждаемого эпоксида при разложении под действием света дифторфосфатов, фосфоро-молибдатов, фосфоровольфраматов, вольфрамогерманатов, силико-вольфраматов, молибдосиликатов диазониев, содержащих в фе-нильном ядре алкокси -, 4-арилмеркапто - или 4-ариламидогруппы [ пат. Среди последних оптимальным сочетанием стабильности и светочувствительности обладают соли 2 5-диалкокси - 4-морфолино - и 2 5-диалкокси - 4-тиотолилфенил - Диазониев. [19]
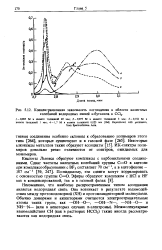 |
Концентрационная зависимость поглощения в области валентных колебаний водородных связей н-бутанола в СС14. [20] |
Кислоты Льюиса образуют комплексы с карбонильными соединениями. По-видимому, эти сдвиги могут коррелировать с основностью группы СО. [21]
Кислоты Льюиса, такие как А1С13, ZnQ2, BF3, SnCl4, дают с простыми эфирами соответствующие оксониевые соединения, которые называют эфиратами. Они, как правило, устойчивы. Например, эфират трифторида бора-жидкость, которая перегоняется без разложения, а эфират тетрахлорида олова - кристаллическое соединение. [22]
Кислота Льюиса используется в количестве, эквимолекулярном ацилирующему агенту, так как после реакции он остается связанным кетоном. [23]
Кислоты Льюиса, такие как А1С13, ZnCl2, BF3, SnCl4, дают с простыми эфирами соответствующие оксониевые соединения, которые называют эфиратами. Они, как правило, устойчивы. Например, эфират трифторида бора-жидкость, которая перегоняется без разложения, а эфират тетрахдорида олова - кристаллическое соединение. [24]
Кислоты Льюиса могут осуществлять атаки на различные гете-роатомы, в результате чего образуются комплексы ( в, г, д, е), часто возникающие в качестве промежуточных при получении карбокатионов. [25]
Кислота Льюиса - любая молекула или частица, способная принимать ( акцептировать) электроны на вакантную орбиталь. В качестве вакантной орбитали выступает, как правило, НСМО. Она может иметь как 0 -, так и я-симметрию. [26]
Кислота Льюиса - любая частица, имеющая вакантную орбиталь и являющаяся акцептором электронов. [27]
Кислоты Льюиса, например Ag, SbF5, BF3, A1C13 и другие, ускоряют реакции 5дД, так как способствуют ионизации субстрата посредством комплексообразования. Этот факт получил название электрофилъный катализ ( см. об этом и в разд. [28]
Кислоты Льюиса образуют со спиртами донорно-акцепторные комплексы, в которых атом кислорода выступает в роли донора НЭП. [29]
Кислоты Льюиса прежде всего увеличивают реакционную способность обычно весьма инертного хлористого водорода по отношению к двойным связям. [30]
Страницы: 1 2 3 4