Кислота - льюис
Cтраница 3
Кислоты Льюиса, такие, как хлористый алюминий, трехфтористый бор, хлорное олово, хлористый цинк и хлорное железо, исключительно важные катализаторы некоторых органических реакций. И обратно, даже слабые основные свойства кислородных и галоидных соединений могут играть решающую роль при определении течения реакций. [31]
Кислоты Льюиса могут давать тот же эффект [ схемы ( 127), ( 128) ]; относительная легкость удаления трет-бутильной группы позволяет в принципе использовать эту группу для защиты определенных положений в кольце. Мета - и napa - крезолы могут быть разделены через их ди-грет-бутильные производные. [32]
Кислоты Льюиса представляют собой соединения с дефицитом электронов в. [33]
Кислоты Льюиса и, следовательно, могут являться катализаторами. Однако было найдено, что в целом кислоты являются гораздо более слабыми катализаторами, чем основания. [34]
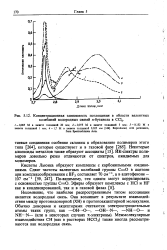 |
Концентрационная зависимость поглощения в области валентных колебаний водородных связей н-бутанола в СС14. [35] |
Кислоты Льюиса образуют комплексы с карбонильными соединениями. По-видимому, эти сдвиги могут коррелировать с основностью группы СО. [36]
Кислоты Льюиса могут быть нескольких типов. [37]
Кислоты Льюиса оказывают существенное влияние на реакции карбонильных соединений с криптооснованиями. Они повышают активность карбонильной группы. Содержащийся в крип-тоосновании атом металла оказывает такое же влияние, что следует учитывать при составлении схем процессов. Этим путем приходят к циклическим переходным состояниям, в которых все электронные переходы могут протекать одновременно. [38]
 |
Восстановление карбонильных соединений алюмогидридом лития. [39] |
Кислоты Льюиса могут изменять специфичность реакций. Так, в присутствии эфирата ВРз, LiAlH4 и NaBH4 восстанавливают сложные эфиры и лактоны до простых эфиров. [40]
Кислоты Льюиса могут давать тот же эффект [ схемы ( 127), ( 128) ]; относительная легкость удаления трег-бутильной группы позволяет в принципе использовать эту группу для защиты определенных положений в кольце. Мета - и napa - крезолы могут быть разделены через их ди-грег-бутильные производные. [41]
Кислоты Льюиса делят на первичные и вторичные. [42]
Более реакционноспособные кислоты Льюиса при комнатной температуре обеспечивают протекание экзотермических реакций как со смолами на основе глици-дилозото эфира, так и с эпоксидироваяными смолами на основе кислот олефинового ряда. Вследствие этого они могут использоваться в качестве отвердителей только для небольших количеств, когда могут допускаться времена жизни, равные примерно 30 сек. При больших массах температура экзотермической реакции довольно велика, что затрудняет возможность их применения. В слу - чае систем, содержащих большое число гидроксильных групп, возможно также, что содержание воды может стать критическим и для удаления воды из системы потребуется повышение температуры. [43]
Кислотами Льюиса считаются галогениды бора, алюминия, кремния, олова, фосфора, мышьяка, сурьмы и многих других элементов, ионы-комплексообразователи Ag, Co3, Сг3, Р12 идр. [44]
Кислотами Льюиса могут быть атом, молекула или катион, обладающие вакантной орбиталью и способные принимать пару электронов с образованием ковалентной связи. Представителями кислот Льюиса служат галогениды элементов второй и третьей групп периодической системы ( BF3, A1C13, FeCl3, FeBr3, ZnCb и др.), катионы металлов, протон. [45]
Страницы: 1 2 3 4