Другая кислота - льюис
Cтраница 1
Другие кислоты Льюиса - А1С13, FeCl3, SnCl4, SbQ3 - либо неэффективны, либо приводят к образованию смеси полимеров, а кислородные кислоты-хлорная, п-полуол-сульфокислота - быстро превращаются в полуэфиры полиэтиленглико-ля. Сокатализатором в этом процессе может служить только сухой HF ввиду низкой нуклеофильности фторид-иона. При использовании трех-фтористого бора в виде эфирата образуются нециклические продукты. [1]
Другие кислоты Льюиса также увеличивают скорость деалкилиро-вания 0-органических производных переходных металлов. [2]
В отличие от других кислот Льюиса хлорид железа образует с хлоранги-дридами наиболее стабильные комплексы, которые в процессе перегонки легко отделяются от хлорангидридов, что обеспечивает высокое качество последних. [3]
Почти такой же эффективностью обладают и некоторые другие кислоты Льюиса ( A1C1S, ZnCl2, AgBF4); HgCla, SnCl4, SbCl3 и TiCU менее эффективны. [4]
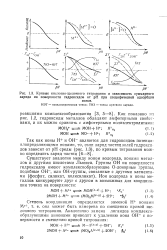 |
Кривые кислотно-щелочного титрования и зависимость суммарного заряда на поверхности гидроксидов от рН при специфической адсорбции. [5] |
Существует аналогия между ионом водорода, ионами металлов и другими кислотами Льюиса. [6]
Известны различные модификации данной реакции, когда в качестве катализаторов используют другие кислоты Льюиса - ZnCI2, FeCI3 и др. В качестве ацилирующих агентов помимо ацилгалогенидов используют ангидриды кислот или нитрилы. [7]
В главе 3 мы рассматривали основания, которые присоединяют протоны или другие кислоты Льюиса по неподелениой электроотрицательного элемента. Поскольку орбнталь, несущую неподеленную пару, принято обозначать как и-орбнталь, такие основания получили название п-основангш или п-донорое электронов. Алканы имеют электроны лишь на с-связях, поэтому их следует считать а-основаниями или с-донорами, Существует еще и третий вид основности, характерный для олефниов, которые можно считать я-основаниями или я-донорами. [8]
Спирты могут быть этерифицнровапы дпазоалканами только в присутствии три-фторида бора или других кислот Льюиса. [9]
Бромная ртуть, выделяющаяся в ходе реакции, образует, как и другие кислоты Льюиса, комплекс с Аг3СВг, что приводит к изменению природы алкилирующего агента. [10]
Поэтому можно было ожидать, что не только протон, но и другие кислоты Льюиса, в частности ионы переходных металлов также смогут координировать аминонитрены с образованием сравнительно стабильных соединений. [11]
Катализаторы Фрпделя - Крафтса - А1С13, BF3, SnCl4, ZnCl2, TiBr4 и другие кислоты Льюиса - используют при низких температурах для получения продуктов высокого молекулярного веса. Все катализаторы Фриделя - Крафтса, применяемые в катпопной полимеризации, требуют присутствия какого-либо сокатализатора, который действует как донор протона. Катализатором может быть вода, органическая кислота и даже органический углеводород. [12]
Аналогичный механизм процессов инициирования, происходящих без сокатализаторов, был предложен для полимеризации в присутствии и других кислот Льюиса. [13]
Удивительно, что только хлорид ( или бромид) алюминия и пентахлорид сурьмы действуют как катализаторы; другие кислоты Льюиса не способствуют галогенированию в ядро. [14]
Хлорирование и бромирование элементарным галогеном в присутствии переносчиков галогена, таких, как А1С13, FeCl3 и другие кислоты Льюиса, также, вероятно, идет через переходное состояние типа 2 на схеме (7.77), поскольку отношение ( 1 / 2 орто) / пара, например при хлорировании, составляет от 0 9 до 1 2, что скорее согласуется с атакой молекулярного хлора, а не катиона галогена ( см. также разд. Часто приводимый в учебниках механизм образования катионов галогена в присутствии переносчиков галогена до сих пор точно не доказан. [15]
Страницы: 1 2 3 4