Другая кислота - льюис
Cтраница 2
К такому заключению приводят данные по изотопному обмену водорода в галоидалкилах с кислотами в присутствии хлористого алюминия и других кислот Льюиса. [16]
Хлорирование происходит очень легко при взаимодействии арена с хлором в присутствии небольших количеств катализатора ( Fe, FeCl3, другие кислоты Льюиса) ( гл. [17]
Ароматический кетон представляет собой более сильное основание Льюиса, чем ацилгалогенид, и образует стабильный комплекс с А1С1з или другой кислотой Льюиса. Кетон выделяют, разлагая его комплекс с А1С1з водой или соляной кислотой. [18]
При электрофильном хлорировании молекулярным хлором в качестве катализатора чаще всего применяют РеС13, а также 12, А1СЬ, TiCU, TlCla, SiO2 и другие кислоты Льюиса. Скорость реакции прямо пропорциональна концентрации субстрата, хлора и катализатора. [19]
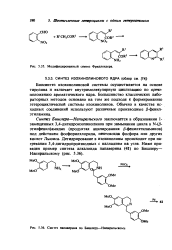 |
Модифицированный синтез Фрилленлера.| Синтез папаверина по Бишлеру-Напиральскому. [20] |
Синтез Бишлера-Напиральского заключается в образовании 1-замещенных 3 4-дигидроизохинолинов при замыкании цикла в N - ( / 3-этилфенил) амидах ( продуктах ацилирования / 3-фенилэтиламинов) под действием фосфорилхлорида, пентоксида фосфора или других кислот Льюиса. Дегидрирование в изохинолины происходит при нагревании 3 4-дигидропроизводных с палладием на угле. [21]
Замещенные виниловые эфиры ( ос-метил - [724, 726, 740, 741], а-этил - [724, 726], ос-н-бутил - [724, 726] и а-фенилвинилэтило-вый эфир [724, 726]) реагируют с ортомуравьиным эфиром только в присутствии хлористого цинка, применение эфирата трехфтористого бора и других кислот Льюиса приводит к осмолению реакционной смеси. Кроме того, для достижения максимальных выходов ( 40 - 65 %) требуется применять избыток ортомуравьиного эфира. [22]
Однако в отличие от других кислот Льюиса, требующих довольно жестких условий проведения реакции, триме-тнлсилилиодид вызывает это превращение уже при комнатной температуре. Благодаря этому обстоятельству, которое, вообще говоря, могло бы показаться второстепенным, метоксигруппа, ранее считавшейся тупиковой для осуществления трансформационных переходов, теперь может рассматриваться как один из удобных вариантов временной защиты спиртовой функции. [23]
Однако в отличие от других кислот Льюиса, требующих довольно жестких условий проведения реакции, триме-тилсилилиодид вызывает это превращение уже при комнатной температуре. [24]
Однако в отличие от других кислот Льюиса, требующих довольно жестких условий проведения реакции, триме-тилсилилиодид вызывает это превращение уже при комнатной температуре. Благодаря этому обстоятельству, которое, вообще говоря, могло бы показаться второстепенным, метоксигруппа, ранее считавшейся тупиковой для осуществления трансформационных переходов, теперь может рассматриваться как один из удобных вариантов временной защиты спиртовой функции. [25]
Так, основания триэтиламин и хинуклидин одинаково легко реагируют с протонами: малый размер протонов позволяет им беспрепятственно подходить к атомам азота и присоединяться к ним. При замене протона на другую кислоту Льюиса - триметилбор ( СН3) 3В картина взаимодействия меняется. [26]
Спирты проявляют свойства не только слабых кислот, но так - же и слабых оснований Льюиса, т.е. они обладают амфипротон-ными свойствами. Дами фосфора, серы или с другими кислотами Льюиса. С сильными минеральными кислотами спирты образуют соли ал-коксония. На этих свойствах основаны многие важные реакции Спиртов, среди которых следует выделить замещение гидроксиль -: ой группы на галоген, т.е. превращение спиртов в алкилгалоге -, дегидратацию спиртов и этерификацию спиртов с помо - ю органических и неорганических кислот и их производных. [27]
Фенолы алкилируются в кольцо под действием самых разнообразных алкилирующих агентов: алкенов, спиртов и алкилгалогенидов в условиях кислотного катализа. Так как фенолы взаимодействуют с галогенидами алюминия и другими кислотами Льюиса с образованием солей типа АгОАЮЬ, в качестве катализаторов предпочитают использовать серную, фтористоводородную, фосфорную кислоты или катиониты КУ-2, даукс и другие катнонообменные смолы. Таким образом, из крезола и изобутилена в промьпплениостн получают пространственио затрудненный фенол - 2 6-ди-трет - бутил-4 - метилфенол ( ионол), который широко применяется для стабилизации полимеров. [28]
В соответствии с рассмотренной выше ролью хлористого алюминия и других кислот Льюиса ( катализаторов Фриделя - Крафтса) как переносчиков, галогена функция этих вспомогательных веществ состоит в том, чтобы поляризовать реагент и усилить тем самым его характер как кислоты Льюиса ( см. стр. [29]
При растворении ароматических углеводородов в жидком фтористом водороде происходит образование другого типа комплексов - о-комплексов. Образованию а-комплексов способствует наличие в системе трехфтористого бора или других кислот Льюиса. В присутствии последних а-комплексы образуются и с хлористым водородом. [30]
Страницы: 1 2 3 4