Другая кислота - льюис
Cтраница 3
Превращение двух a - комплексов в диоксан идет через циклическое переходное состояние. Кроме галогенов процессам циклизации в условиях низких температур способствуют BF3 и другие кислоты Льюиса. При низких температурах удалось получить циклические макроэфиры, содержащие до восьми атомов кислорода в молекуле. [31]
Каталитическое разложение диазосоединений проходит через карбеноиды [ см., например, схему ( 42) ], что обнаруживается по различному составу продуктов, получаемых из карбеноидов меди и свободных карбенов. Катализаторами служат медь и ее соли, разнообразные галогениды металлов и другие кислоты Льюиса, а также тетрафенилэтан. [32]
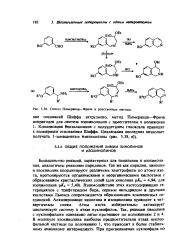 |
Синтез Померанца-Фрича и родственные методы. [33] |
Большинство реакций, характерных для хииолинов и изохинолинов, аналогичны реакциям пиридинов. Взаимодействие этих азотсодержащих ге-тероциклов с трифторидом бора, серным ангидридом и другими кислотами Льюиса сопровождается образованием комплексных соединений. Алкилирование хинолина и изохинолина приводит к четвертичным солям. Атом азота избирательно активирует циклическую систему к атаке нуклеофилов. В молекуле изохинолина наиболее предпочтительна атака нуклео-фильной частицы по положению 1, что приводит к более стабильному анионному интермедиату. [34]
 |
Структурные параметры и полные энергии для реакции Н - НаСОа. [35] |
Координата реакции - симметрии Cs, и продукт имеет плоскость симметрии. Таким же образом, помимо протона, будут присоединяться к кислороду многие другие кислоты Льюиса. Присоединение слабых нуклеофилов к карбонильной группе усиливается за счет таких взаимодействий. [36]
Бензол и его гомологи хлорируются, бромируются и иодируются. Реакции способствуют катализаторы, поляризующие молекулу галогена: галогениды железа, алюминия и другие кислоты Льюиса. Иногда к реакционной смеси просто добавляют железные опилки. [37]
Наиболее часто ацетили-рование моносахаридов проводится уксусным ангидридом в пиридине на холоду или же уксусным ангидридом в присутствии ацетата натрия. Реже применяется ацетилирование уксусным ангидридом при нагревании в присутствии кислых катализаторов: хлористого цинка ( или других кислот Льюиса), серной или хлорной кислот. Во всех случаях можно достичь исчерпывающего ацетилирования, но в зависимости от условий результаты могут несколько отличаться в отношении содержания таутомерных форм. [38]
Спирты проявляют свойства не только слабых кислот, но также и слабых оснований Льюиса, т.е. они обладают амфипротонными свойствами. Как основания Льюиса спирты образуют донорно-акцепторные комплексы с галогенидами и оксигалогенидами фосфора, серы или с другими кислотами Льюиса. С сильными минеральными кислотами спирты образуют соли алкоксония. На этих свойствах основаны многие важные реакции спиртов, среди которых следует выделить замещение гидроксильной группы на галоген, т.е. превращение спиртов в алкилгалогениды, дегидратацию спиртов и этерификацию спиртов с помощью органических и неорганических кислот и их производных. [39]
Электрофильным агентом в реакции Вильсмейера является хлориминиевая соль, образующаяся при взаимодействии диметилформамида и хлорокиси фосфора или другой кислоты Льюиса. [40]
Это может означать, что либо в определяющей скорость стадии не происходит заметного растяжения связи углерод - галоген, либо, если оно происходит, что дополнительная энергия, необходимая для растяжения связи углерод - фтор, более чем компенсируется выигрышем энергии, большим для фторида, чем для хлорида, в любом другом процессе. Такое объяснение является, кажется, более уместным; выигрыш энергии, вероятно, происходит при электрофильном катализе А1С13 или какой-нибудь другой кислотой Льюиса. [41]
Ацетали кетонов более чувствительны к действию кислых агентов. Поэтому в качестве катализатора присоединения кеталей к виниловым эфирам обычно рекомендуется использовать хлорное железо [44], впрочем, можно применять также хлористый цинк, эфи-рат трехфтористого бора и другие кислоты Льюиса. [42]
Этим способом синтезируют многие конденсированные циклические системы. Полифосфорная кислота - один из наиболее широко применяемых катализаторов для внуримолеку-лярного ацйлирования по Фриделю - Крафтсу ( что определяется ее высокой эффективностью); в качестве катализаторов можно брать и А1С1з, серную кислоту, другие кислоты Льюиса и протонные кислоты, хотя реакции ацйлирования ацилгало-генидами обычно не катализируются протонными кислотами. [43]
Нефтяные сульфиды образуют стабильные комплексы донорно-акцепторного типа с галогенами, галоген-ал килам и ( метилиодидом и др.), с солями металлов - олова, серебра, ртути, алюминия, цинка, титана, галлия и другими кислотами Льюиса за счет передачи неподеленной пары электронов атома серы на свободную электронную орбиталь акцептора. Важнейшие комплексообразователи - хлорид алюминия, тетрахлорид титана, хлорид ртути ( II), ацетат серебра, карбонилы железа. Реакции комплексообразования не селективны, в той или иной степени они протекают и с другими типами гетер оатомных соединений. Однако в сочетании с другими физико-химическими методами ком-плексообразование служит важным инструментом установления состава, строения сульфидов. [44]
Ряд методов получения днхлорангидридов фосфонистых кислот основан на использовании треххлористого фосфора. Арилди-хлорфосфины можно синтезировать из ароматических соединений и треххлористого фосфора. Обычно лучшие результаты получаются при применении хлористого алюминия или других кислот Льюиса. [45]
Страницы: 1 2 3 4