Адсорбированная кислота
Cтраница 2
Откачка образца при 250 G приводила к удалению полос поглощения только молекулярно адсорбированной кислоты. [16]
Число основных центров на чистом сахарном угле определяли [23] путем измерения количества адсорбированной кислоты, например бензойной, уксусной и соляной, в водной среде. [17]
Объяснить, почему в опыте 1 при одинаковой концентрации уксусной кислоты процент адсорбированной кислоты в колбах 2 и 3 различен. [18]
Узкая полоса поглощения с максимумом при 1700 слГ1 характерна для карбонильной группы молекулярно адсорбированной кислоты. Промывание двуокиси титана растворителем приводит к исчезновению из спектра полосы поглощения при 1700 см-1, что свидетельствует об удалении с поверхности молекулярно адсорбированной кислоты. Полоса поглощения карбоксилат-иона после промывания не изменяет интенсивности. [19]
 |
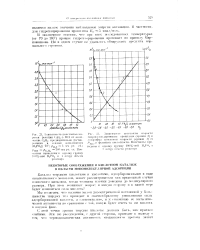
Возможные ориентации молекул ВПД на поверхности SiO2 при малых ( / и близких к монослойному ( / / заполнениях поверхности. [20] |
При адсорбции кислот на поверхности SiO2 следует учитывать возможность протекания реакции этерификации между адсорбированной кислотой и небольшой частью поверхностных ОН-групп. При этом образуется достаточно стабильное поверхностное соединение, устойчивое до 300 - 350 С. Реакция с АК или МАК может служить удобным способом модификации поверхности SiO2 винилсодержащими функциональными группами для дальнейшего проведения прививочной полимеризации. [21]
Недостатком двух последних схем является отсутствие объяснения корреляции между количествами поглощенного молекулярного кислорода и адсорбированной кислоты. [22]
Различная адсорбируемость кислотных и основных компонентов на поверхности электрода приводит к изменению констант диссоциации адсорбированных кислот и оснований по сравнению с их величинами в объеме раствора. Его наряду с изменением приэлектродной концентрации заряженных веществ необходимо принимать во внимание при определении констант скорости приэлектродных поверхностных химических реакций. [23]
Вне зависимости от того, справедливы или нет высказанные соображения о причине значительного изменения удельной активности адсорбированных кислот, из двух приведенных экспериментальных примеров вытекает, что в качестве меры каталитической активности твердых кислотных контактов не может быть, в общем случае, использована кип-цен т рация подвижных протонов, обычно легче всего определяемая опытным путем. [24]
Мы полагаем, что наличие малой диэлектрической постоянной у большинства твердых тел приводит к скачкообразному уменьшению силы адсорбированной кислоты, а следовательно, и к снижению ее каталитической активности но сравнению с той, какую будет иметь та же кислота в жидкой фазе. [26]
Найдено, что если шерсть сначала обработать раствором рацемической л-метоксиминдальной кислоты, а затем экстрагировать водой, то адсорбированная кислота, постепенно разделяясь на антиподы, перейдет в раствор. [27]
Мыла образуют на поверхности металлов пленки, обладающие большей прочностью, по сравнению со слоями, образованными только адсорбированными кислотами. [28]
Данные об адсорбции уксусной кислоты из водного раствора древесным углем выражены через равновесную молярную концентрацию, отнесенную к количеству адсорбированной кислоты в расчете на грамм древесного угля. Проверьте эти данные при помощи уравнений Ленгмюра и Фрейндлиха. [29]
Найдено, что если шерсть сначала обработать раствором рацемической n - метоксиминдальной кислоты, а затем экстрагировать водой, то адсорбированная кислота, постепенно разделяясь на антиподы, перейдет в раствор. [30]
Страницы: 1 2 3 4