Недиссоциированная кислота
Cтраница 1
Недиссоциированная кислота всегда присоединяется по двойной связи. В присутствии буферного бората ( рН 10) хлоргидрин практически не образуется, между тем как в кислой среде ( рН 4 7) наступает хлоргидринирование. Увеличение диссоциации равносильно уменьшению выхода хлоргидрина. [1]
Концентрация недиссоциированной кислоты ( HCN) не включена в уравнение, так как молекулы кислоты не несут заряда. [2]
Коэффициент активности недиссоциированной кислоты обычно принимают равным единице. [3]
Поверхностно-активным веществом является недиссоциированная кислота НХ. При этом CHX должна быть пропорциональна С, а не С2, поскольку при используемых низких концентрациях рН остается постоянным и равным рН растворителя. [4]
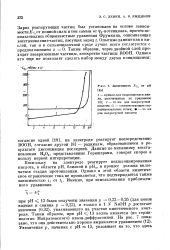 |
Зависимость Еу2 от рН. [5] |
Поскольку на электроде реагирует недиссоциированная кислота, в области рН, близкой к рНа, в процесс должна включаться стадия протонизации. [6]
Реакция может быть катализирована и недиссоциированной кислотой или кислотой Льюиса. В этих случаях положительный заряд на углеродном атоме карбонильной группы увеличивается в результате образования водородной связи или координации с катализатором. [7]
 |
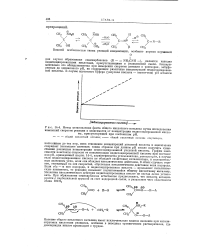
Метод установления факта общего кислотного катализа путем исследования изменений скорости реакции в зависимости от концентрации недисеоциированнои кислоты, присутствующей при постоянном рН. [8] |
График зависимости константы скорости от концентрации недиссоциированной кислоты при постоянном рН, приведенный на рис. 14 - 4, характеризуется углом наклона, равным нулю, в случае если недиссоциированная кислота не обладает свойствами катализатора, и положительным значением угла, если она обладает каталитическим действием. В обоих случаях отрезок, отсекаемый на оси скоростей, обусловлен каталитическим действием иона водорода. Если оба - и ион водорода, и недиссоциированная кислота - проявляют каталитическую активность, то реакцию называют подчиняющейся общему кислотному катализу. Механизм каталитического действия недиссоциированных кислот не всегда легко установить. [9]
 |
Метод установления факта общего кислотного катализа путем исследования изменений скорости реакции в зависимости от концентрации недиссоциированной кислоты, присутствующей при постоянном рН. [10] |
График зависимости константы скорости от концентрации недиссоциированной кислоты при постоянном рН, приведенный на рис. 14 - 4, характеризуется углом наклона, равным нулю, в случае если иедиссоциированная кислота не обладает свойствами катализатора, и положительным значением угла, если она обладает каталитическим действием. В обоих случаях отрезок, отсекаемый на оси скоростей, обусловлен каталитическим действием иона водорода. Если оба - и ион водорода, и недиссоциированная кислота - проявляют каталитическую активность, то реакцию называют подчиняющейся общему кислотному катализу. Механизм каталитического действия недиссоциированных кислот не всегда легко установить. [11]
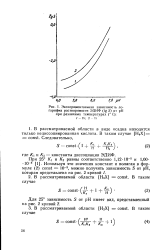 |
Экспериментальная зависимость логарифма растворимости ЭДИФ ( lg 5 от рН при различных температурах ( С. [12] |
В рассматриваемой области в виде осадка находится только недиссоциированная кислота. [13]
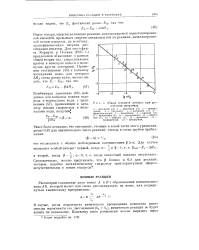 |
Общий основной катализ при разложении нитрамида. [14] |
Иначе говоря, энергия активации реакции, катализируемой недиссоциированной кислотой, превышает энергию активации той же реакции, катализированной ионом водорода, на величину, пропорциональную энергии диссоциации кислоты. Для этого факта Хориути и Полный ( 1935 г.) предложили объяснение в рамках О общей теории сил, удерживающих протон в молекуле воды и в молекулах других оснований. [15]
Страницы: 1 2 3 4