Обобщенная кислота
Cтраница 4
В растворителях, неспособных к образованию полноценных водородных связей, лишние молекулы субстрата могут участвовать в стабилизации ионных промежуточных продуктов, что может приводить к появлению аномальных стехиометрии кислотно-основного равновесия типа обсуждаемого в разд. Катализируемые обобщенными кислотами - основаниями реакции в протонных растворителях могут протекать через перенос протона вдоль цикла связанных водородными связями молекул растворителя, начинаясь и кончаясь на реагирующей функциональной группе. Некоторые примеры иллюстрируют эти эффекты. [46]
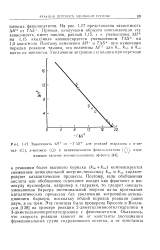 |
Зависимость Д / / от - Г AS для реакций гидразина с п-ме. [47] |
ОК характеризуют каталитические процессы. Поэтому, если обобщенная кислота или обобщенное основание входит как фрагмент в молекулу нуклеофила, например в гидразин, то следует ожидать уменьшения барьера потенциальной энергии из-за протекания каталитических процессов без увеличения энтропийно-актива-ционного барьера, поскольку общий порядок реакции равен двум, а не трем. Эта гипотеза была проверена Брюсом и Виллисом [138] на примере реакции 2-диметиламиноэтилгидразина и 3-диметиламииопропилгидразина с фенилацетатом. [48]
Каков же физический смысл этого понятия в случае шлаков, которые практически не содержат указанных ионов. Ответ на этот вопрос дает теория обобщенных кислот Льюиса, которая не связывает понятие кислоты или основания с какими-либо определенными соединениями, а исходит из особенностей электронного строения данного вещества. По Льюису кислота - это молекула, атом или ион, способные присоединить пару электронов и таким путем образовать ковалентную связь с основанием. Последнее является также атомом, ионом или молекулой, которые могут предоставить такую общую пару электронов. Приведенное определение включает в себя и обычные представления о кислотах и основаниях. [49]
Многочисленные примеры, перечисленные выше, доказывают правильность вывода о том, что обобщенные кислоты и основания трудно расположить в определенной последовательности по их относительной силе. Однако известны случаи, когда к обобщенным кислотам и основаниям применимо уравнение Бренстеда и функция кислотности Гамметта. [50]
Страницы: 1 2 3 4