Арилстибиновая кислота
Cтраница 2
Методом Барта - Шмидта были синтезированы многие арилстибиновые кислоты. [16]
Этот прием приложим в основном к получению арилстибиновых кислот, содержащих нитрогруппу [1], и не имеет общего значения для всех электро-ноакцепторных заместителей. Так, фенил-4 - стибиновая-1 - арсиновая кислота получается с хорошим выходом и в щелочном растворе. [17]
Не удалось получить пиридиниевых: солей некоторых о-замещенных арилстибиновых кислот ( которые в этих условиях легко диспропорционируются), а также кислот, содержащих омы-ляющиеся кислотами заместители типа амидной группы. [18]
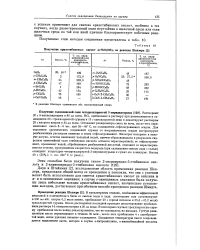
В табл. 9 приводятся сведения о некоторых арилстибиновых кислотах, синтезированных реакцией Шмидта. [19]
В патентной литературе рекомендуется следующий общий способ получения арилстибиновых кислот по реакции Шеллера. [20]
В ароматическом ряду хорошо изучены реакции галоидоводородных кислот с арилстибиновыми кислотами, приводящие к образованию тетрагалогенидов арилсурьмы, и реакции гидролиза последних в арилстибиновые кислоты. Эти процессы широко используются для очистки и выделения арилстибино-вых кислот. Значительно менее подобные реакции изучены в алифатическом ряду. Образующиеся при этом соединения типа RSbClg ( acac) и соответственно RSbGl3Ox, где асасН - ацетилацетон, ОхН - 8-оксихинолин, по данным УФ -, ИК - и ПМР-спектров, содержат шестикоор-динированный атом сурьмы, с чем, вероятно, и связано повышение их устойчивости к термическому и гидролитическому воздействиям. [21]
Исходя из этих данных, а также из результатов анализов арилстибиновых кислот, Шмидт заключил, что они имеют в твердом состоянии строение тримеров I, где х - число ассоциированных молекул воды, которое может меняться в зависимости от способа получения кислоты. [22]
По окончании выделения азота прибавляют при перемешивании воду до объема 6 л, арилстибиновую кислоту отфильтровывают, тщательно промывают водой и сушат на воздухе. Затем кислоту суспендируют в 100 - 200 мл конц. Реакционную смесь охлаждают до - 20 С, прибавляют при перемешивании 5 М раствор хлористого олова до полноты осаждения арилдихлорстибина. [23]
Даук и Штейнман [76] разработали общий способ получения пиридиние-вых солей арилпентахлорантимонатов, с успехом использованный для очистки и характеристики арилстибиновых кислот; на большом числе примеров показано, что перекристаллизация пиридиниевых солей из смеси спирта и соляной кислоты приводит к аналитически чистым веществам, обладающим характерной температурой плавления ( см. гл. Выделение чистых стибиновых кислот из таких солей проводят действием разбавленного раствора соды с последующим подкислением образующегося раствора. [24]
Существенным преимуществом реакции Несмеянова является то, что при этом не образуется больших объемов стойкой пены, как при синтезе арилстибиновых кислот по методу Шмидта, а также и то, что ароматические соединения трехвалентной сурьмы, получающиеся по методу Несмеянова, гораздо легче очищаются и идентифицируются, чем арил - и диарилстибиновые кислоты. [25]
В ароматическом ряду хорошо изучены реакции галоидоводородных кислот с арилстибиновыми кислотами, приводящие к образованию тетрагалогенидов арилсурьмы, и реакции гидролиза последних в арилстибиновые кислоты. Эти процессы широко используются для очистки и выделения арилстибино-вых кислот. Значительно менее подобные реакции изучены в алифатическом ряду. Образующиеся при этом соединения типа RSbClg ( acac) и соответственно RSbGl3Ox, где асасН - ацетилацетон, ОхН - 8-оксихинолин, по данным УФ -, ИК - и ПМР-спектров, содержат шестикоор-динированный атом сурьмы, с чем, вероятно, и связано повышение их устойчивости к термическому и гидролитическому воздействиям. [26]
Реакция проводится в ацетоне или этилацетате и приводит к образованию в качестве главных продуктов моно-арильных соединений сурьмы, выделенных ( с хорошими выходами) в виде моноарилстибиноксидов и арилстибиновых кислот. [27]
 |
Получение арилстибиновых кислот ArSbO ( OH2 uo реакции Шеллера. [28] |
Даук и Штейнман [2], исследовавшие область применения реакции Шеллера, предложили общий метод ее проведения и показали, что она с успехом может быть использована для синтеза арилстибиновых кислот из анилина и м - и и-замещенных анилинов; в случае о-замещенных анилинов были получены лишь небольшие выходы арилстибиновых кислот, значительно уступающие выходам, достигаемым при обычном способе проведения реакции Шмидта. [29]
Приведенные в табл. 11 результаты синтеза сурьмяноорганических соединений по методу двойных диазониевых солей показывают, что при этом получаются главным образом соединения трехвалентной сурьмы, легче очищаемые и идентифицируемые, чем арилстибиновые кислоты. Метод быстрее в проведении и компактнее в аппаратурном оформлении, и при его осуществлении не наблюдается обильного пенообразования и выделения труднофильтрующихся осадков, что характерно для реакции Шмидта. [30]
Страницы: 1 2 3 4