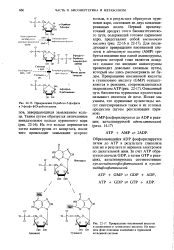
Инозиновая кислота
Cтраница 1
Инозиновая кислота может превратиться затем в адениловую и гуанило-вую кислоты. Вся последовательность реакций, приводящих от рибозо-5 - фос-фата к инозиновой кислоте, изображена на фиг. Источники различных атомов кольцевой системы пуринов, указанные на фиг. [1]
Инозиновая кислота придает пищевым продуктам вкус мяса. Она является сложным соединением. [2]
Инозиновая кислота отличается от адениловой только тем, что в ней вместо аденина содержится гипоксантин. Образование инозиновой кислоты при дезаминировании адениловой кислоты происходит в мышечной ткани. [3]
Аминирование инозиновой кислоты с образованием адениловой протекает в два этапа, очень сходно с синтезом 5-аминоимидазол - 4-карбоксамид-рибо - нуклеотида ( уравнения XVIII. Весьма вероятно, что фермент, катализирующий отщепление фумаровой кислоты от аденилосукцината - аденилосукциназа - катализирует также и аналогичную реакцию, описываемую уравнением ( XVIII. Существенно, что для реакции образования аденилоянтарной кислоты ( на пути синтеза аденин-нуклеотидов) в качестве кофермента требуется ГТФ. В то же время при синтезе гуанин-нуклеотидов, как мы увидим ниже, роль кофермента играет АТФ. Отсюда естественно следует вывод о регуляторной функции этих соединений: ясно, что избыток ГТФ должен сдвигать синтез в сторону образования АТФ и, наоборот, при избытке АТФ должно синтезироваться больше ГТФ. [4]
Превращение инозиновой кислоты в гуаниловую также протекает в два этапа. [5]
Превращение инозиновой кислоты в гуаниловую кислоту зависит от промежуточного образования ксантозин-5 - фосфата в результате окислительных процессов, протекающих при участии НАД и дегидрогеназы. При переносе амидного азота глутамина на С2 ксантиловой кислоты образуется гуанозин-5 - фосфат, вероятно, при одновременном взаимодействии ксантиловой кислоты с АТФ и глутамином. В бактериальных системах источником аминогруппы служит не глутамин, а аммиак ( ср. [6]
Схема биосинтеза инозиновой кислоты показана на фиг. [7]
Процесс биосинтеза инозиновой кислоты из рибозо-5 - фосфа-та довольно сложен и идет через несколько стадий. Основные реакции этого процесса показаны на схеме ( стр. [8]
Для последующего превращения инозиновой кислоты в адениловую кислоту ( AMP) требуется введение еще одной аминогруппы, донором которой тоже является аспар-тат; однако это введение аминогруппы происходит довольно сложным путем, который мы здесь рассматривать не будем. [10]
Заключительный этап биосинтеза инозиновой кислоты состоит в присоединении еще одного остатка муравьиной кислоты от новой молекулы формилтетрагидрофолиевой кислоты к 5-ами-но - 4-имидазолкарбоксамидрибонуклеотиду с образованием 5-формамидо - 4-имидазолкарбоксамидр ибонуклеотида и тетра-гидрофолиевой кислоты. [11]
Первым выделенным мононуклеотидом была инозиновая кислота ( IMP, 9), которая была получена из гидролизата мяса Ли-бихом в 1847 г. примерно за 20 лет до выделения нуклеиновых кислот из гнойных клеток Мишером. Инозиновая кислота не является широкораспространенным в природе нуклеотидом; она образовалась в процессе выделения по Либиху за счет дезаминирования AMP, который сам по себе был выделен из мышц лишь в 1927 г. Были выделены все обычные нуклеотиды аденина, цитозина, гуанина, тимина и урацила, так же как и многие минорные нуклеотиды, например, образующиеся из псевдоуридина, дигидроуридина и метилированных производных аденозина и гуанозина. [12]
Синтез адениловой кислоты из инозиновой кислоты идет в две стадии через аденилянтарную кислоту. Донатором азота является аспарагиновая кислота. Эта первая реакция во MHOHJIVB напоминает реакцию ( 8) синтеза инозиновой кислоты. Основное различие состоит в используемых макроэргических соединениях, которые дают энергию для синтеза С-N связи. На второй стадии от аденилян-тарной кислоты отщепляется фумаровая кислота и образуется адениловая кислота ( стр. [13]
Биосинтез гуаниловой кислоты из инозиновой кислоты также идет в две стадии и такжо требует затраты энергии. На первой стадии инозиновая кислота окисляется до ксантиловой кислоты; при помощи восстановленного никотинамид-аденин-динуклеоти-да. Эта реакция катализируется ферментом и н о з и н - 5 - ф о с-фатдегидрогеназой. На второй стадии происходит аминирование ксантиловой кислоты, которое требует затраты энергии. Донатором азота здесь является глутамин. Реакция катализируется ксантозин-5 - фосфат-глутамин-амидолигазой, В результате реакции образуется гуаниловая кислота, аденозин-монофосфат и пирофосфорная кислота ( стр. [14]
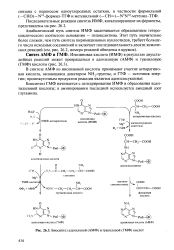 |
Биосинтез адениловой ( АМФ и гуаниловой ( ГМФ кислот. [15] |
Страницы: 1 2 3 4