Индивидуальная кислота
Cтраница 1
Выделенные индивидуальные кислоты ( рис. 2) соответствуют действующим стандартам и могут использоваться в различных отраслях народного хозяйства. [1]
Себестоимость индивидуальной кислоты Cj0 - 2-изопропил - 5-метил - 2-гексе-новой ( а-изопропил-р-изобутилакриловой) кислоты, полученной из изобутилена, в 2 раза ниже себестоимости неодекановой кислоты, синтезированной по методу Коха. [2]
Концентрация индивидуальных кислот в масле была выбрана таковой, чтобы кислотное число масла было порядка 1 мг КОН / г. Концентрация мыл нафтеновых кислот ( нафтенатов) в масле составляла примерно 0 1 % по весу. Все опыты проводились в запаянных стеклянных сосудах, в которых пространство над поверхностью масла было заполнено азотом. В каждый сосуд помещалось 60 г кабельной бумаги или артона, предварительно высушенных и пропитанных трансформаторным маслом, и заливалось 140 г масла, содержащего исследуемый продукт. [3]
Для получения индивидуальных кислот нормального строения использовалась товарная фракция СЖК Сю-С ] 6 ( СТУ 6 - 02 - 105 - 62), содержащая около 10 % непредельных соединений и столько же изо-кислот. [4]
Установки для получения индивидуальных кислот С [ - С запроектированы на Уфимском НПЗ им. [5]
На примере эфиров любой индивидуальной кислоты, например терефталевой или изофталевой, можно проследить, как увеличение объема боковых заместителей во всех случаях приводит к повышению дипольного момента пластификаторов. Это, по-видимому, обусловлено стерическими препятствиями взаимной компенсации диполей соседних молекул. [6]
Для этерификации ДЭГ индивидуальными кислотами от С5 до С9 энергия активации изменяется от 3 27 до 14 86 ккал / моль и для реакции этих же кислот с ТЭГ от 6 23 до 14 82 ккал / моль. Небольшие изменения энергии активации образования эфиров индивидуальных кислот, например, капроновой и ДЭГ ( Е 10 55 ккал / моль без катализатора и Е 8 90 ккал / моль в присутствии КУ-2), можно объяснить тем, что в отсутствие катализатора протекает каталитическая реакция с участием водородных ионов, образовавшихся за счет диссоциации карбоксильных групп. В присутствии катализатора реакция протекает значительно бысрее за счет повышения концентрации водородных ионов. Более низкие значения энергий активации образования эфиров ТЭГ и высокомолекулярных кислот по сравнению с ДЭГ, видимо, можно объяснить влиянием большей основности триэтиленгликоля. [7]
Для этерификации ДЭГ индивидуальными кислотами от С5 до С9 энергия активации изменяется от 3 27 до 14 86-ккал / моль и для реакции этих же кислот с ТЭГ от 6 23 до 14 82 ккал / моль. Небольшие изменения энергии активации образования эфиров индивидуальных кислот, например, капроновой и ДЭГ ( Е 10 55 ккал / моль без катализатора и Е 8 90 ккал / моль в присутствии КУ-2), можно объяснить тем, что в отсутствие катализатора протекает каталитическая реакция с участием водородных ионов, образовавшихся за счет диссоциации карбоксильных групп. В присутствии катализатора реакция протекает значительно бысрее за счет повышения концентрации водородных ионов. Более низкие значения энергий активации образования эфиров ТЭГ и высокомолекулярных кислот по сравнению с ДЭГ, видимо, можно объяснить влиянием большей основности триэтиленгликоля. [8]
В отличие от серной кислоты индивидуальные кислоты ( без со-катализатора) в мягких условиях, по-видимому, не инициируют катионную полимеризацию циклосилоксанов. Реакция полимеризации имеет первый порядок по мономеру и переменный порядок по катализатору. При концентрации НС1 больше 1 2 - 10 - 2 моль / л скорость полимеризации уменьшается с увеличением содержания хлористого водорода, и реакция имеет второй порядок по хлорному железу. [9]
Таким образом, возможность определения индивидуальных кислот и оснований лимитируется как константой диссоциации определяемой кислоты или основания, так и концентрацией этих веществ в растворе. [10]
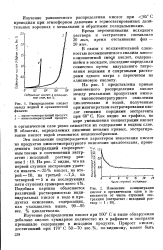 |
Распределение кислот между водной и органической фазами.| Изменение концентрации кислот в органическом слое в зависимости от числа ступеней экстракции ( экстрагент. исходный раствор 1. 10. [11] |
Подобная картина объясняется различной растворимостью индивидуальных кислот в воде и продуктах окисления, содержащих, как указывалось выше, 90 - 95 вес. [12]
Канифоль так же, как и индивидуальные кислоты, входящие в ее состав, способна на многие реакции, присущие исходным смоляным кислотам. [13]
Приведены константы скорости этерификации диэтиленгликоля и индивидуальных кислот в присутствии набухшего в различных реагентах катионита КУ-2. Показано, что набухание катионита при 125 - 140 С в диэтиленгликоле улучшает его эффективность, как катализатора этерификации. [14]
Промышленном масштабе как низшие, так и высшие индивидуальные кислоты. [15]
Страницы: 1 2 3 4