Межмолекулярное колебание
Cтраница 2
Причина больших трудностей применения метода модельных расчетов к описанию межмолекулярных колебаний по сравнению с внутримолекулярными состоит в следующем В выражения частот внутримолекулярных колебаний силовые постоянные межмолекулярных связей и углов ( К, К & и К) входили лишь как небольшие поправки к достаточно точно найденным силовым постоянным валентных ОН-связей и угла НОН. Поэтому правильная оценка даже порядка величин силовых постоянных К и К для описания внутримолекулярных колебаний воды оказывается уже достаточной. Совершенно иная картина возникает при анализе межмолекулярных колебаний, частоты которых целиком определяются силовыми постоянными самой водородной связи и прилежащих к ней углов. Очевидно, что в этом случае для вычисления абсолютных значений таких частот грубые оценки силовых постоянных углов Р и у оказываются совершенно непригодными. Поэтому, исследуя поведение частот либрационных колебаний воды в разных комплексах, приходится вводить дополчи-тельные упрощения и ограничиваться более общим рассмотрением, когда в результате расчета находится лишь относительное расположение полос. [16]
RiAH или BR2), плоскостью, которая содержит координату межмолекулярного колебания собственно водородной связи ЕАН... [17]
В спектрах воды и ионных растворов неупругая компонента характеризует частоты межмолекулярных колебаний. Таким образом, наиболее интенсивные линии в спектрах соответствуют в основном движениям, связанным с водородными группами. [18]
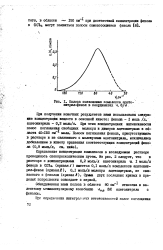 |
Полоса поглощения комплекса ацето - нитрил-фенол в координатах - 4, 8 / - 0. [19] |
Обнаруженная нами полоса в области 80 см 1 отнесена к валентному межмолекулярному колебанию Ч нв ВС ацетонитрила с фенолш. [20]
Однако, если комплекс имеет более низкую симметрию Cv большинство его межмолекулярных колебаний сопровождается одновременно изменением и углов, и связей. В таких случаях для характеристики колебаний совершенно неприменимы распространенные в обиходе понятия либр анионных и трансляционных колебаний, а необходимо строгое указание их форм. Вычисление формы, как мы увидим ниже, необходимо во всех случаях, когда речь идет даже о грубой оценке интенсивности полос поглощения или о их смещении на 20 - 100 см-г. Иными словами, вычисление формы колебания оказывается неотъемлемой частью почти любого современного спектрохимического исследования. [21]
Теоретически найдена формула, описывающая зависимость интенсивности от частоты в спектре межмолекулярных колебаний жидкости, состоящей из анизотропных молекул. Методами классической статистики произведен учет вклада случайных изменений фаз и броуновских переориентации. Сопоставление с экспериментом позволило оценить молекулярные параметры, лежащие в основе теории, в частности, важнейший из них - частоту случайных ( некогерентных) взаимодействий молекул. [22]
При средних или повышенных температурах ( для многоатомных жидкостей) уменьшение энергии межмолекулярных колебаний в результате замещения легкого изотопа тяжелым вызывает увеличение энергии разрыва межмолекулярных связей, а уменьшение энергии ван-дер-ваалъсо-вого взаимодействия при таком замещении вызывает уменьшение энергии разрыва межмолекулярных связей. Выше показано, что разность энергии колебаний изотопных молекул сравнительно быстро уменьшается с ростом температуры и молекулярного веса. Поэтому в области стандартной термодинамической температуры влияние изотопного замещения на энергию разрыва межмолекулярных связей неассоциированных жидкостей обычно определяется различием энергии ван-дер-ваальсового взаимодействия изотопных молекул. Это подтверждается тем, что разности теплот парообразования некоторых дейтеропроизводных углеводородов и их соответствующих обычных аналогов, рассчитанные по экспериментальным данным о температурной зависимости давления пара, близки к разностям ван-дер-ваальсовой энергии для тех же соединений, рассчитанным как описано выше. [23]
С помощью уравнений ( 10) и ( И) легко вычислить частоту межмолекулярных колебаний и ее температурную зависимость для тяжелого льда. Соответствующая кривая приведена на рис. 4, из которого видно, что для изотопического изменения частоты колебаний О - - О при высоких температурах получается правильное значение. Вычисленная температурная зависимость к ( Т) для тяжелого льда оказывается еще более слабой, чем для легкого, как и должно быть вследствие убывания коэффициента ангармоничности х - / к5 / 4е с увеличением массы ( 5 - [ J. Поэтому параллельный ход экспериментальных прямых ш ( Т) для легкого и для тяжелого льда остается непонятным. [24]
Эффекты, связанные с влиянием ионов на рентгеновские РФР, неупругие спектры частот межмолекулярных колебаний и на диффузионные процессы, в данном обзоре обсуждаться не будут. [25]
Наряду с этим ясно, что в области температур, где влияние нулевой энергии межмолекулярных колебаний на их амплитуды или влияние структуры жидкости ( ассоциации посредством водородных связей) на плотность мало, изотопный эффект в мольном объеме определяется различием ван-дер-ваальсового взаимодействия изотопных молекул. Таким образом, увеличение мольного объема при замещении водорода дейтерием как в воде, так и в бензоле для температур выше 200 С, вплоть до соответствующих критических точек, может быть объяснено только ослаблением ван-дер-ваалъсового взаимодействия при указанном замещении. [26]
Показано, в частности, что если, как обычно в растворах, средняя частота межмолекулярных колебаний среды заметно меньше частоты колебаний А - - В, то полоса v ( AH) при образовании комплекса А - Н - - В расширяется в меньшей степени, чем при равенстве этих частот. Такой эффект связан с понижением степени стохастичности колебательного движения А-В. [27]
Показано, в частности, что если, как обычно в растворах, средняя частота межмолекулярных колебаний среды заметно меньше частоты колебаний А - - В, то полоса v ( АН) при образовании комплекса А - Н - - В расширяется в меньшей степени, чем при равенстве этих частот. Такой эффект связан с понижением степени стохастичности колебательного движения А - - В. [28]
В случае плоских va и неплоских vv деформационных колебаний молекул ROH, а также их некоторых межмолекулярных колебаний, когда последние нехарактеристичны по форме, соотношение ( 31) выполняется только приблизительно. В таких молекулах при замене даже одного атома Н на D смещается иногда целая группа полос поглощения. [29]
После рассмотрения основных структурных моделей воды и водных растворов анализируются возможности этих методов для определения структуры межмолекулярных колебаний, влияния ионов на структуру растворителя и, наконец, механизма и параметров самодиффузии. При чтении второго раздела, посвященного вопросам теории, могут возникнуть определенные трудности, так как он подразумевает знание элементов квантовой механики, теории рассеяния и статистической физики. Желающие разобраться в этих вопросах более серьезно могут обратиться к дополнительной литературе, список которой помещен в конце главы. В третьем разделе содержится описание аппаратуры и способов обработки экспериментальных данных. Большой интерес представляет собой четвертый раздел, где обстоятельно изложены результаты эксперимента и приведено их обсуждение. [30]
Страницы: 1 2 3 4