Количество - прореагировавшее вещество
Cтраница 2
При протекании этих реакций количество прореагировавшего вещества пропорционально количеству света. Второй тип фотохимических реакций характеризуется большими значениями квантового выхода. Эти реакции возбуждаются светом и далее идут счень быстро; все они являются экзотермическими. [16]
И в этом случае количество прореагировавшего вещества возрастает с концентрацией нитрата, но еще значительно медленнее, чем это имело место при возрастающих концентрациях альдегида. [17]
Обозначим через X - количество прореагировавшего вещества, а - начальное количество вещества, а - реакционная поверхность каждого зародыша. [18]
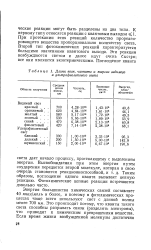 |
Длины воли, частоты и энергии видимого и ультрафиолетового света. [19] |
При протекании этих реакций количество прореагировавшего вещества пропорционально количеству света. Второй тип фотохимических реакций характеризуется большими значениями квантового выхода. Эти реакции возбуждаются светом и далее идут очень быстро; все они являются экзотермическими. [20]
Числитель последней дроби пропорционален количеству прореагировавшего вещества, а знаменатель равен затраченной энергии. Следовательно, ф является мерой количества вещества, прореагировавшего на единицу затраченной энергии. Как видно из табл. 10, при изких давлениях ( 10 мм рт. ст.) и малых силах тока разряд малоэффективен для всех углеводородов; с ростом этих величин ф становится примерно одинаковым для всех углеводородов. [21]
Выделение реакционного тепла, пропорционального количеству прореагировавших веществ, делает возможным определение протяженности зоны реакции по изменению температуры ДХЭ по высоте реактора. Уровень, на котором прекращается рост температуры, соответствует полной утилизации хлора из ДХЭ, то есть верхней границе зоны реакции. [22]
Тепловой эффект химического превращения определяется количеством прореагировавших веществ и удельным тепловым эффектом реакции. [23]
Скорость химической реакции принято выражать количеством прореагировавшего вещества в единицу времени. Однако в условиях школы определение концентрации реагирующих веществ затруднительно, мало наглядно и трудно понимаемо, поэтому мы сочли возможным рекомендовать учительству демонстрацию опытов по скорости химической реакции не по количеству израсходованного, а по количеству полученного вещества в единицу времени. [24]
Как видно из табл. 7, количество прореагировавшего вещества контролировалось двумя независимыми методами. [25]
При помощи радиоактивных индикаторов легко определять количество прореагировавшего вещества, однако в данном случае метод меченых атомов только облегчает эксперимент. Значительно важнее определять константы скорости обратимых реакций при равновесии, так как в этом случае только метод меченых атомов может разрешить эту проблему. [26]
Как известно, экспоненциальный закон нарастания количества прореагировавшего вещества ( или образования конечного продукта) действительно наблюдается во многих случаях при окислении углеводородов в газовой фазе. [27]
Численное значение константы скорости реакции равно количеству прореагировавшего вещества в единицу времени, если концентрации реагирующих веществ равны по 1 молю. [28]
Соотношение между количеством поглощенной энергии и количеством прореагировавшего вещества впервые было установлено К. А. Тимирязевым, доказавшим, что эти количества строго подчиняются закону сохранения энергии. Эйнштейн вывел формулу, являющуюся математическим выражением закона фотохимической эквивалентности, согласно которому каждая молекула, реагирующая под действием света, поглощает только один квант световой энергии. Следовательно, в любой элементарной реакции может принимать участие только один квант света, т.е. число прореагировавших молекул должно равняться числу поглощенных квантов. [29]
Соотношение между количеством поглощенной энергии и количеством прореагировавшего вещества выражается законом фотохимической эквивалентности, который был выведен ( 1912) термодинамическим путем Эйнштейном и является по существу выражением закона сохранения энергии применительно к рассматриваемым процессам. По этому закону каждая молекула, реагирующая под действием света, поглощает один квант радиации, вызывающий реакцию. [30]
Страницы: 1 2 3 4