Количество - гидроперекись
Cтраница 2
Возможно, что до момента образования некоторого количества гидроперекиси металлический катализатор не принимает активного участия в окислении. [16]
Таким образом, выход уксусной кислоты определяется количеством гидроперекиси, образовавшейся в первой стадии. Когда гидроперекись израсходуется, то образование уксусной кислоты прекратится, хотя концентрация непрореагировавшего ацетальдегида будет еще велика. В данном случае предельный выход объясняется вполне убедительно. В других случаях данные о существовании макростадий удается получить далеко не всегда. [17]
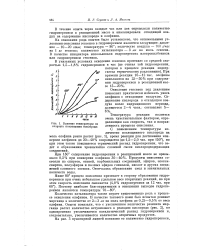 |
Влияние температуры на скорость поглощения кислорода. [18] |
В течение опыта через каждые час или два определяли количество гидроперекиси в реакционной массе и анализировали отходящий воздух на содержание кислорода и олефинов. [19]
Поскольку эта реакция должна происходить с большой скоростью, аналитически определимых количеств гидроперекиси в системе может не накапливаться. [20]
Однако для большинства алкенов количество поглощенного кислорода значительно выше, чем количество накопившейся гидроперекиси. [21]
Для того чтобы обеспечить преобладание кумилпероксиради-калов в системе, надо ввести такое количество гидроперекиси кумила, при котором скорость реакции продолжения цепи ( W0jWl / 2) не зависит от концентрации гидроперекиси. [22]
Этот способ полимеризации дает возможность получать полистиролы с заданными свойствами путем регулирования количества гидроперекиси, температуры и способа введения в реакционную сферу окислительно-восстановительной системы. [23]
В поисках удовлетворительного объяснения возможного механизма реакции проведены опыты по изучению влияния количества гидроперекиси на выход а-оксикетонов, исследованы превращения возможных промежуточных продуктов с гидроперекисью в присутствии катализатора. Удалось установить, что увеличение дозировки гидроперекиси выше 2 молей на 1 моль олефина не приводит к существенному возрастанию выходов а-оксикетонов. [24]
Интересно, что в большинстве случаев молярное количество образующихся кетона и спирта больше, чем количество распавшейся гидроперекиси. По мнению авторов, это связано с окислением циклогексана, используемого в качестве растворителя, гидроперекисью. [25]
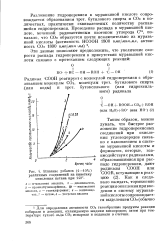 |
Влияние добавок ( 4 - 10 %. [26] |
Разложение гидроперекиси в муравьиной кислоте сопровождается образованием трет, бутилового спирта и ССЬ в количествах, практически эквивалентных количеству распавшейся гидроперекиси. Проведение распада в муравьиной кислоте, меченной радиоактивным изотопом углерода С14, показало, что GO2 образуется почти исключительно из муравьиной кислоты ( активность НСООН 1800 имп / мин. [27]
Смесь из реактора поступает в холодильник, где охлаждается до начальной температуры t, после чего часть ее, соответствующая количеству гидроперекиси, поданной на разложение, выводится из системы, а оставшаяся часть возвращается на циркуляцию. Как уже говорилось, в качестве реакционной среды может быть использована либо разбавленная серная кислота, легко отстаивающаяся от продуктов разложения гидроперекиси и возвращаемая в производственный цикл, либо собственно смесь продуктов разложения гидроперекиси. [28]
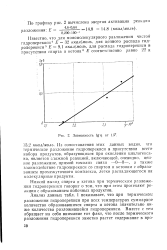 |
Зависимость lgr от 1 / Т. [29] |
Анализ данных табл. 1 показывает, что при термическом разложении гидроперекиси при всех температурах суммарное количество образовавшихся спирта и кетона значительно ниже количества разложившейся гидроперекиси. [30]
Страницы: 1 2 3 4