Количество - гидроперекись
Cтраница 4
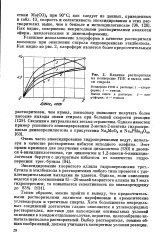 |
Влияние растворителя на конверсию ГПК и выход окиси стирола. [46] |
Очень часто эпоксидирование гидроперекисями ведут, используя в качестве растворителя избыток исходного олефина. Этот прием применен для получения окиси циклооктена [130] и диоки-си 4-винилциклогексена, где циклооктен и 1 2-эпокси - 4-винилцик-логексан берутся с двукратным избытком от количества гидроперекиси трет. [47]
При разложении оксидата л-цнмола ( окисление при 135 - 140СС до содержания гидроперекиси в оксидате 18 - 20 %) количество выделенной куми-но вой кислоты равнялось 20 - 25 % от всего количества гидроперекиси, взятой на разложение. [48]
Реакция окисления первичных аминов 97 - 98 является характерной реакцией гидроперекисей. При действии гидроперекиси уксусной кислоты при охлаждении окисление останавливается на образовании нитрозосоединения; если же процесс ведется без охлаждения и в концентрированном растворе, то реакция протекает весьма бурно, и при этом образуются также нитросоединения. Изменяя количества гидроперекиси уксусной кислоты, можно соответственно влиять на образование вторичных продуктов окисления аминов, на получение азо - и азоксисоединений. [49]
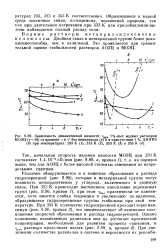 |
Зависимость динамической вязкости и ] див 1 % - ных водных растворов. [50] |
Различие обнаруживается и в кинетике образования и распада гидроперекисей ( рис. 9.90), которые в метакрильной группе могут возникать непосредственно у углерода, включенного в двойную связь. При 313 К происходит постепенное накопление перекисных групп ( рис. 9.90, кривая 1), при этом т Д 111 практически не изменяется, хотя имеется слабая тенденция к увеличению: по-видимому, образующиеся гидроперекисные группы стабильны при этой температуре. При 353 К количество гидроперекисей проходит через максимум ( рис. 9.90, кривая 2), что свидетельствует об изменении соотношения скоростей образования и распада гидроперекисей. [51]
Более полное представление об отдельных стадиях процесса окисления полипропилена дает анализ вторичных продуктов реакции. В начале процесса окисления в полимере накапливаются гидроперекиси и в незначительном количестве образуются карбонильные группы и летучие вещества. По мере повышения количества гидроперекисей начинает возрастать содержание летучих, а также карбонильных и спиртовых групп, причем одновременно увеличивается число двойных связей и падает молекулярный вес полимера. На последних стадиях реакции происходит накопление кислот и образуются окись и двуокись углерода. [52]
В присутствии меркаптанов резко возросла коррозия меди. При окислении изопропилбензола в присутствии дисульфидов обнаружено некоторое количество гидроперекисей и карбоновых кислот. [53]
Характерной особенностью гидроперекиси является ее ограниченная растворимость в реакционной смеси. Поэтому гидроперекись, оставленная стоять при комнатной температуре, выделяется в значительной массе в форме кристаллов. При охлаждении от - 8 до - 10 С может быть выделено - - - 50 % всего количества гидроперекиси, образовавшейся при окислении углеводорода. Гидроперекись п - ( грег-бутилизопропилбензола) представляет собой бесцветные блестящие тонкие пластинки с температурой плавления 61 - 62 С. Гидроперекись легко растворяется в обычных органических растворителях за исключением петролейного эфира, из которого она может быть перекристаллизована. Она количественно реагирует с растворами йодистого калия в ледяной уксусной кислоте и довольно быстро взаимодействует с щелочными растворами сульфита натрия, превращаясь при этом в карбинол, плавящийся при 78 - 79 С. [54]
Возможно, что в этом случае катализатор теряет свою активность, в самом процессе инициирования цепей, например при реакции с гидроперекисью. При малых концентрациях стеарата меди ( 1 - - 8) - 10 5 молъ / л практически весь поглощенный кислород превращается в гидроперекись и ускорение реакции связано именно с накоплением гидроперекиси. При больших концентрациях катализатора ( 10 - 4 - 10 - 2 молъ / л) происходит интенсивный распад перекиси, количество накопившейся гидроперекиси намного меньше количества поглощенного кислорода. Замедление реакции связано с дезактивацией катализатора, так как введение дополнительного количества стеарата меди приводит к кратковременному ускорению процесса. Дополнительное введение гидроперекиси в этилбензол, содержащий стеарат меди ( 6 35 - 10 - 5 молъ / л), как это ни странно, замедляет реакцию. [55]
Возможно, что в этом случае катализатор теряет свою активность, в самом процессе инициирования цепей, например при реакции с гидроперекисью. При малых концентрациях стеарата меди ( 1 н - 8) - 10 - 5 молъ / л практически весь поглощенный кислород превращается в гидроперекись и ускорение реакции связано именно с накоплением гидроперекиси. При больших концентрациях катализатора ( 10 - 4 - 10 - 2 молъ / л) происходит интенсивный распад перекиси, количество накопившейся гидроперекиси намного меньше количества поглощенного кислорода. Замедление реакции связано с дезактивацией катализатора, так как введение дополнительного количества стеарата меди приводит к кратковременному ускорению процесса. Дополнительное введение гидроперекиси в этилбензол, содержащий стеарат меди ( 6 35 - 10 - 5 молъ / л), как это ни странно, замедляет реакцию. [56]
Страницы: 1 2 3 4