Тиофеновое кольцо
Cтраница 1
Тиофеновое кольцо не гидрируется до тех пор, пока из него не удалится сера, хотя первая стадия реакции может включать одновременно и удаление атома серы и присоединение двух атомов водорода. [1]
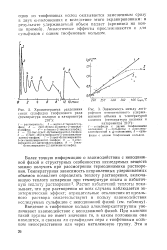
Пятичленпое тиофеновое кольцо с атомом серы и: дпумя двойными сопряженными связями по многим свойствам напоминает шестпчленпое карбоциклнческое ( бензольное) кольцо с тремя сопряженными двойными связями. [2]
Пятичленное тиофеновое кольцо с атомом серы и двумя двойными сопряженными связями по многим свойствам напоминает шестичлен-ное карбоциклическое ( бензольное) кольцо с тремя сопряженными двойными связями. Подобная же аналогия наблюдается и в свойствах соответствующих гомологических рядов тиофена, в которых тиофеновое кольцо конденсировано с одним или несколькими бензольными кольцами или нафталиновыми ядрами, с гомологами конденсированных ди - и полициклических ароматических углеводородов. Близость свойств высокомолекулярных гомологов конденсированных ароматических углеводородов с аналогичными им по структуре углеродного состава серусодержащими производными ароматических углеводородов и обусловливает трудность разделения этих двух классов соединений, содержащихся в высших фракциях нефтей. [3]
Пятичленное тиофеновое кольцо с атомом серы и двумя двойными сопряженными связями по многим свойствам напоминает шестичлен-ное карбоциклическое ( бензольное) кольцо с тремя сопряженными двойными связями. Подобная же аналогия наблюдается и в свойствах соответствующих гомологических рядов тиофена, в которых тиофеновое кольцо конденсировано с одним или несколькими бензольным кольцами или нафталиновыми ядрами, с гомологами конденсированных ди - и полициклических ароматических углеводородов. Близость свойств высокомолекулярных гомологов конденсированных ароматических углеводородов с аналогичными им по структуре углеродного состава серусодержащими производными ароматических углеводородов и обусловливает трудность разделения этих двух классов соединений, содержащихся в высших фракциях нефтей. [4]
Тиофеновое кольцо ФДБТ более устойчиво, чем сульфиды и, по-видимому. Возможно, некоторое расщепление тиофенового кольца в условиях коксования происходит в результате атаки атома в кольце радикалами с последующим образованием сульфидподобного соединения и разрывом С. [5]
Природа тиофенового кольца, в частности, геометрические особенности этого гетероцикла, позволяет рассматривать его в реакциях как жесткую группу с ее влиянием на направленность процесса внутримолекулярного замыкания. [6]
Замыкание тиофенового кольца при наличии в бензольном кольце молекулы ( фенилтио) уксусной кислоты группы CN в орго-положении к группе SCH2COONa происходит еще легче, чем при наличии карбоксильной группы ( ср. [7]
Образование тиофенового кольца протекает легко, как и в случае производных хлоруксусной кислоты. [8]
Введение в тиофеновое кольцо алкилмеркаптогруппы увеличивает взаимодействие с неподвижной фазой. При наличии такой группы не имеет значения то, в каком положении она находится, и связана ли сульфидная сера с тиофенозым кольцом непосредственно или через метиленовую группу. [10]
Каталитическое восстановление тиофенового кольца или заместителей в тио-феновом цикле осложнено двумя факторами: отравлением катализатора и возможностью протекания конкурентного гидрогенолиза, восстановительного элиминирования атома серы, особенно при использовании никеля Ренея. Действительно, при использовании тиофенов в качестве темплатов, на которых строится структура, в конце синтетической последовательности часто прибегают к десульфуризации, что может служить важной синтетической стратегией ( цругие примеры см. разд. [11]
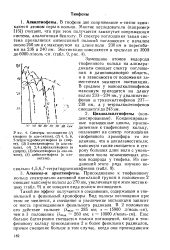
Присоединение к тиофеновому кольцу спектрально активной винильной группы в положении 2 смещает максимум полосы до 270 нм, увеличивая при этом экстинк-цию ( табл. 9) и не изменяя вида полосы поглощения. [13]
Соединения с тиофеновым кольцом при достаточно большом числе конденсированных ароматических ядер ( 3 и более) переходят в неситякой кокс. [14]
Замещение в тиофеновом кольце в значительной степени зависит от присутствия атома серы. [15]
Страницы: 1 2 3 4